
Asam Asetat
Misalnya, karena asam asetat memiliki nilai pKa kira-kira 4,7, ketika pH sama dengan pKa, rasio asetat terhadap asam asetat adalah 1:1. Untuk asam lain, seperti hidrofluorik (HF), yang memiliki nilai pKa sekitar 4,0, ketika pH sama dengan 4,0, rasio ion fluorida terhadap asam hidrofluorik akan menjadi 1:1. Solusi penyangga. Larutan penyangga.

Pembahasan Asam Asetat Rumus Kimia, Karakteristik, dan Manfaatnya
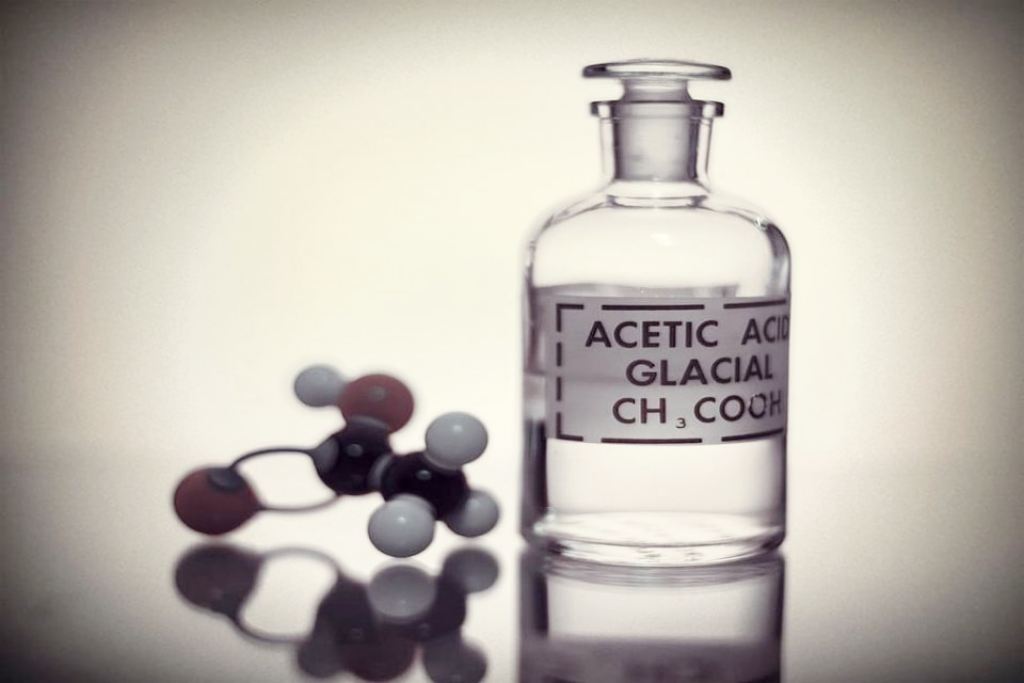
Asam asetat, asam etanoat atau asam cuka adalah salah satu senyawa organik yang berada dalam golongan asam alkanoat. Asam asetat pekat (disebut asam asetat glasial) adalah cairan higroskopis tak berwarna, dan memiliki titik beku 16,7°C. Asam asetat adalah komponen utama cuka (3-9%) selain air. Asam asetat berasa asam dan berbau menyengat.

What Is pKa in Chemistry? Acid Dissociation Constant
Larutan buffer dibuat dari asam asetat 1 M dan natrium asetat 1 M. Tentukan pH larutan tersebut (Ka asam asetat = 1.76 x 10-5) Jawabannya. Tahap 1 .. Tentukan pH larutan ketika 25 mL larutan asam asetat 0.2 M dicampurkan dengan 35 mL larutan NaOH 0.1 M (diketahui pKa asam asetat = 4.752) Tahap 1. Tentukan mol masing masing larutan.

Jual Asam Asetat CH3COO
pKa Definition. pK a is the negative base-10 logarithm of the acid dissociation constant (K a) of a solution. pKa = -log 10 K a. The lower the pKa value, the stronger the acid. For example, the pKa of acetic acid is 4.8, while the pKa of lactic acid is 3.8. Using the pKa values, one can see lactic acid is a stronger acid than acetic acid.

Asam Asetat food grade / Asam Cuka / Glacial 99,85 / Cuka Murni bisa COD Lazada Indonesia
melaminium (+1) mengingat pKa asam asetat = 4,76; sedang pKa melamin berturut-turut: pKa 1 = 5,10 > pKa asam asetat, pKa 2 = 0,20 < pKa asam asetat, dan pKa 3 = -2,10 (Weinstabl dkk, 2001). Perbedaan struktur molekul yang diakibatkan oleh perbedaan rasio molar reaktan tentu saja akan

Asam asetat glasial
General Info. pKa is an acid dissociation constant used to describe the acidity of a particular molecule. Its value is directly related to the structure of the given compound. The constant changes depending on the solvent the compound is used in. Typically, organic chemists compare the various values from their determination in water, DMSO and.

Gambar 1. Pembentukan Asam Asetat dan Asam Laktat dalam Fermentasi... Download Scientific Diagram
Asam asetat adalah contoh zat ini. Nilai pKa larutan dalam DMSO dan pelarut lainnya dapat dijumpai di Acidity-Basicity Data in Nonaqueous Solvents. Superasam adalah asam kuat meskipun dalam pelarut dengan konstanta dielektrik rendah. Contoh superasam adalah asam fluoroantimonat dan asam ajaib.
Asam Asetat Fungsi, Dosis, Efek Samping, dll DokterSehat
Menurut Andriani dan Kurniawati ( 2007), besarnya nilai pKa, yaitu besarnya molekul yang tidak dapat terdisosiasi dipengaruhi oleh kemampuan antibakteri dari asam organik (asam laktat dan asam asetat). Asam asetat memiliki aktivitas antimikroba yang lebih tinggi dibandingkan asam laktat karena nilai pKa asam asetat lebih besar daripada asam laktat.

Perhatikan kurva titrasi larutan asam asetat dengan larut...
Konstanta disosiasi asam. Konstanta disosiasi asam (K a) atau konstanta keasaman adalah sebuah konstanta atau tetapan keseimbangan spesifik untuk sebuah asam dan basa konjugasinya di sebuah larutan berair. [1] Konstanta ini merupakan konstanta kesetimbangan untuk suatu reaksi kimia. yang dikenal sebagai disosiasi dalam konteks reaksi asam-basa.
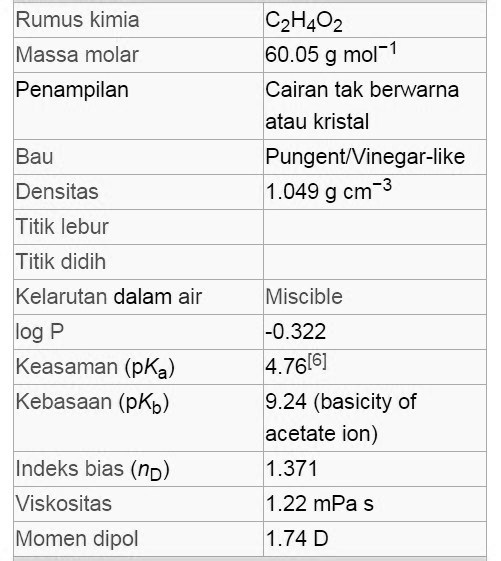
Rumus Kimia Asam Asetat Rumus Kimia
Asam asetat yang pekat merupakan cairan higroskopis yang tak berwarna dan memiliki titik beku 16,7°C. Asam asetat ialah salah satu asam karboksilat paling sederhana dan mempunyai rumus kimia CH3COOH. Asam asetat memiliki sifat korosif terhadap berbagai macam logam seperti besi, serta seng dan magnesium, membentuk gas hidrogen dan garam-garam.

Asam Asetat 6 (1x500 mL) PT One Medika
Definisi pKa. pKa adalah logaritma basa-10 negatif dari konstanta disosiasi asam (K a) larutan. pKa = -log 10 K a Semakin rendah nilai pKa, semakin kuat asamnya. Misalnya, pKa asam asetat adalah 4,8, sedangkan pKa asam laktat adalah 3,8. Dengan menggunakan nilai pKa, seseorang dapat melihat asam laktat adalah asam yang lebih kuat daripada asam asetat.

Sop Pembuatan Larutan Asam Asetat PDF
Diketahui pKa asam asetat = 4,76. Catatan: Larutan penyangga dikatakan baik bila dapat mempertahankan pHnya bila ∆pH = 1,00. Perhitungan kapasitas bufer Kapasitas bufer adalah jumlah asam/basa kuat monoprotik yang harus ditambahkan ke dalam 1 L larutan bufer sehingga terjadi perubahan 1 satuan pH.

Asam Asetat Glacial 1 liter PT Rajawali Mulia Abadi
Berikut adalah tabel nilai Ka umum asam lemah dan rumusnya. Menu. Rumah. Sains, Teknologi, Matematika. Memilih asam atau basa di mana pKa mendekati pH yang dibutuhkan memberikan hasil. Pada titik tengah pada kurva ekivalen, pH = pKa. Ka dari Asam Lemah. Ka dari Asam Lemah; Nama: Rumus: K a: pK a: asetat: HC2H3O2 _ _ _ _ _ 1,8 x 10 -5: 4.7.
:max_bytes(150000):strip_icc()/what-is-pka-in-chemistry-605521_FINAL2-9fdfc39e9aa34caa96d6e74a2c687707.png)
pKa Definition in Chemistry
Membuat asam asetat dengan fermentasi aerob dari alkohol. 2. Membandingkan produk asam asetat yang terbentuk dengan vaariabel sari buah, kadar vinegar dan pH, serta waktu fermentasi. 3. Membiakan starter asam asetat dengan menggunakan mikroba. 4. Membuat inokulum untuk bahan dasar pembuatan asam asetat. Tinjauan Pustaka II.1.

Asam Asetat Toko Alat Peraga
Terlihat bahwa nilai pKa asam asetat memiliki nilai yang mendekati pH buffer tersebut. Oleh karena itu, asam Asetat dan garamnya digunakan pada perhitungan ini. 2. Jika Sanikun ingin mengubah pH buffer pada praktikumnya tetapi Sanikun tidak ingin nilai perubahannya tidak lebih dari 0.1 satuan untuk penambahan 1mmol asam ataupun basa.
Asam Asetat Obat Apa? Dosis, Fungsi, dll. • Hello Sehat
Acetic acid / ə ˈ s iː t ɪ k /, systematically named ethanoic acid / ˌ ɛ θ ə ˈ n oʊ ɪ k /, is an acidic, colourless liquid and organic compound with the chemical formula CH 3 COOH (also written as CH 3 CO 2 H, C 2 H 4 O 2, or HC 2 H 3 O 2). Vinegar is at least 4% acetic acid by volume, making acetic acid the main component of vinegar apart from water. It has been used, as a.