
Berikut data titik beku (Tf) beberapa larutan elektrolit
Berikut adalah contoh soal materi sifat koligatif larutan kelas 12 semester 1 serta jawabannya. 1. Semua sifat berikut tergolong sifat koligatif larutan, kecuali.. A. Penurunan Tekanan Uap. B. Kenaikan Titik Didih. C. Penurunan Titik Beku. D. Tekanan Osmosis. E. Kepekatan Larutan.

Rumus titik beku larutan
Titik beku heksana, yang merupakan senyawa hidrokarbon alifatik, adalah sekitar -95 derajat Celsius atau -139 derajat Fahrenheit. 18.Hidroklorida (HCI) Titik beku larutan asam hidroklorida tergantung pada konsentrasi. Sebagai contoh, larutan 20% HCl memiliki titik beku sekitar -27 derajat Celsius atau -16.6 derajat Fahrenheit. 19.Helium

Cara Menghitung Tetapan Penurunan Titik Beku Larutan (Kf) (UN Kimia 2018 No. 24) YouTube
Meskipun sifat koligatif melibatkan larutan, sifat koligatif tidak bergantung pada interaksi antara molekul pelarut dan zat terlarut, tetapi bergatung pada jumlah zat terlarut yang larut pada suatu larutan. [3] Sifat koligatif terdiri dari penurunan tekanan uap, kenaikan titik didih, penurunan titik beku, dan tekanan osmotik.
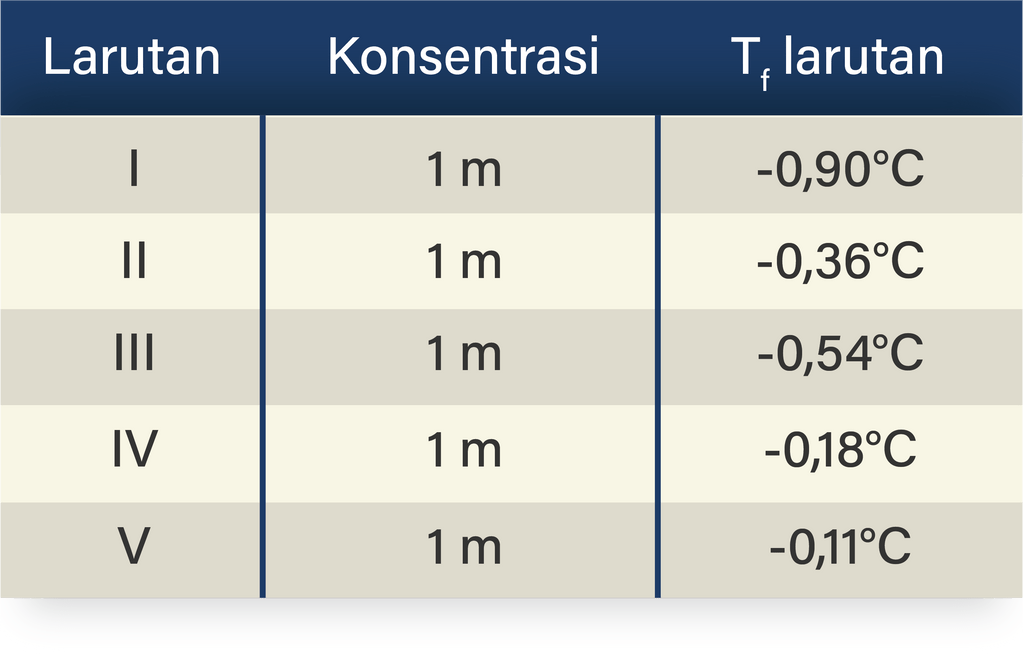
Berikut ini data titik beku beberapa larutan dalam...
Tf larutan (Tb) = Titik beku larutan (°C) Tf pelarut (Tb°) = Titik beku pelarut (°C) ΔTf = Penurunan titik beku (°C) m = Molalitas larutan (molal). Jadi, larutan yang isotonik dengan C6H12O6 0,3 M adalah larutan CaCl2 0,1 M. 4. Tekanan uap jenuh air pada suhu 28⁰C adalah 100 mmHg. Apabila 30 gram urea (Mr=60) dilarutkan dalam 2 mol.
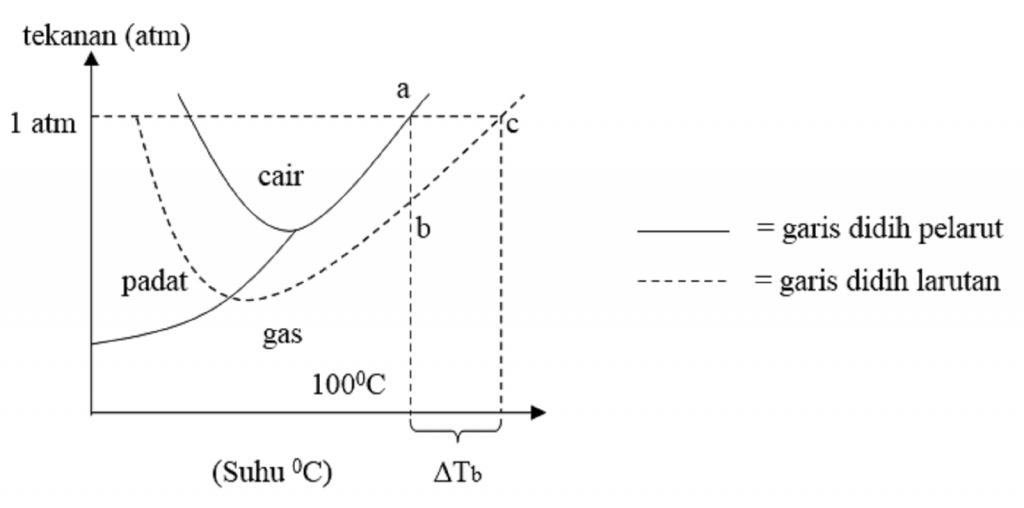
Sifat Koligatif Larutan Kenaikan Titik Didih Dan Penurunan Titik Beku Reverasite
LAPORAN PRAKTIKUM KIMIA PENURUNAN TITIK BEKU LARUTAN. Titik beku adalah suhu dimana tekanan uap cairan sama dengan tekanan uap padatannya. Titik beku larutan lebih rendah daripada titik beku pelarut murni. Hal ini disebabkan zat pelarutnya harus membeku terlebih dahulu, baru zat terlarutnya. Jadi larutan akan membeku lebih lama daripada pelarut.

Larutan berikut yang memiliki titik beku paling tinggi ad...
Penurunan titik beku adalah selisih antara titik beku pelarut dengan titik beku larutan. Penurunan titik beku ini termasuk salah satu sifat koligatif larutan. Dalam perhitungan kimia, penurunan titik beku disimbolkan dengan ΔT f (f berasal dari kata freeze) atau ΔT b . Peristiwa penurunan titik beku ini sering diterapkan pada negara-negara.

Larutan 0,1 molal berikut yang memiliki titik beku terend...
Contoh soal 4. Suatu zat nonelektrolit (Mr = 40 g/mol) sebanyak 30 gram dilarutkan kedalam 900 gram air, titik beku larutan ini adalah - 1,550 C. Berapa gram zat tersebut yang harus dilarutkan kedalam 1,2 kg air agar diperoleh larutan dengan titik beku setengahnya dari titik beku diatas.
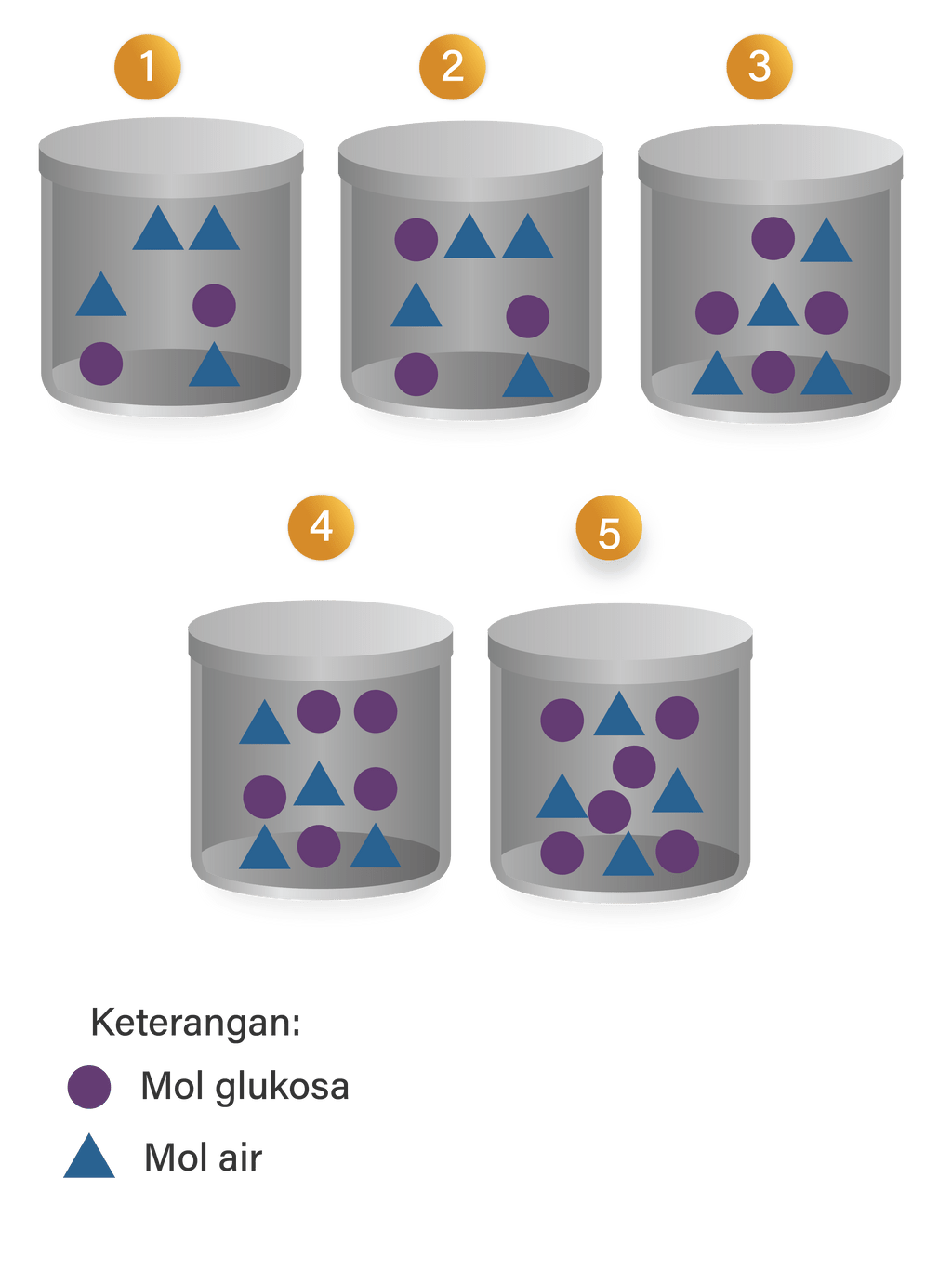
Perhatikan bagan berikut Larutan yang mem...
Penurunan titik beku adalah salah satu sifat koligatif larutan yang dipengaruhi oleh beberapa faktor. Faktor-faktor yang mempengaruhi penurunan titik beku meliputi: Konsentrasi Partikel Terlarut: Semakin tinggi konsentrasi partikel terlarut dalam larutan, semakin besar penurunan titik beku yang terjadi. Ini berarti larutan dengan konsentrasi.

Perhatikan diagram PT air, larutan urea 0,1 m dan NaC...
Sifat koligatif larutan adalah sifat-sifat yang hanya bergantung pada jumlah (kuantitas) partikel zat terlarut dalam larutan dan tidak bergantung pada jenis atau identitas partikel zat terlarut - tidak peduli dalam bentuk atom, ion, ataupun molekul. Sifat koligatif merupakan sifat yang hanya memandang "kuantitas", bukan "kualitas".

Larutan yang memiliki titik beku paling rendah adalah.
Titik beku larutan lebih rendah pelarut murni. Titik beku adalah suhu saat suatu zat menjadi beku di bawah tekanan 1 atm. Misalnya air, air adalah pelarut murni yang memiliki titik beku 0°C. Artinya, air yang awalnya cair akan berubah menjadi padat pada suhu 0°C. Dilansir dari Thought Co, larutan memiliki titik beku yang lebih rendah daripada.

Praktikum Penurunan Titik Beku Pada Pembuatan Es Krim II Sifat Koligatif Larutan YouTube
Misalnya, titik beku normal air adalah 0 o C. Akan tetapi, dengan adanya zat terlarut pada suhu 0 o C, air bisa mejadi belum membeku. Selisih titik beku pelarut (Tf o) dengan titik beku larutan (Tf) yang kemudian disebut penurunan titik beku (ΔTf). Berikut rumus penurunan titik beku: ΔTf = Tf° - Tf

Data percobaan penurunan titik beku Larutan Konsentrasi
Persamaan Penurunan Titik beku. Penurunan titik beku dapat dihitung menggunakan persamaan Clausius-Clapeyron dan hukum Raoult. Dalam larutan ideal encer titik beku adalah: Titik beku larutan total = Titik beku larutan - ΔTf. dimana ΔTf = molalitas * Kf * i. K f = konstanta titik beku air (1,86 ° C kg / mol ) i = Faktor Van't Hoff.

Contoh Soal Titik Beku Larutan (Sifat Koligatif Larutan Elektrolit) YouTube
Pengertian dan Rumus Penurunan Titik Beku Menurut Rananda Vinsiah dalam Fenomena Sifat Koligatif Larutan Kimia Kelas XII (2020, hlm. 19), titik beku merupakan kondisi ketika tekanan uap suatu cairan sama dengan tekanan padatannya. Pada kondisi seperti itu, cairan akan mulai membeku. Seandainya ada suatu zat terlarut yang dicampurkan ke pelarut murni, akan tercipta larutan baru.

Contoh Soal Perbandingan Penurunan Titik Beku (Sifat Koligatif Larutan Elektrolit) YouTube
Sifat koligatif larutan itu ada empat macam, yaitu p enurunan tekanan uap (Δ P), penurunan titik beku (Δ Tf), kenaikan titik didih. Contoh dari larutan nonelektrolit adalah larutan gula seperti glukosa, sukrosa dan maltosa, larutan urea (CON 2 H 4), serta larutan alkohol seperti metanol,.

Berikut disajikan data percobaan tentang titik beku beber...
Dalam persamaan di atas, T F adalah titik beku normal dari pelarut murni (273 K untuk air, contohnya); a liq adalah aktivitas pelarut dalam larutan (aktivitas air untuk larutan berair); ΔH fus T F adalah perubahan entalpi fusi dari pelarut murni pada T F, yaitu 333.6 J/g untuk air pada 273 K; ΔC fus p adalah perbedaan antara kapasitas panas.

Penurunan Titik Beku Larutan Adalah Reverasite
Kemudian, adanya penurunan tekanan uap jenuh larutan akan mengakibatkan penurunan titik beku larutan. Dapat dikatakan bahwa, larutan akan membeku pada temperatur yang lebih rendah. Baca Juga: Pengertian Senyawa Polimer. Nah, berdasarkan penjalasan tadi, dapat dinyatakan bahwa penurunan titik beku larutan adalah selisih antara titik beku pelarut.