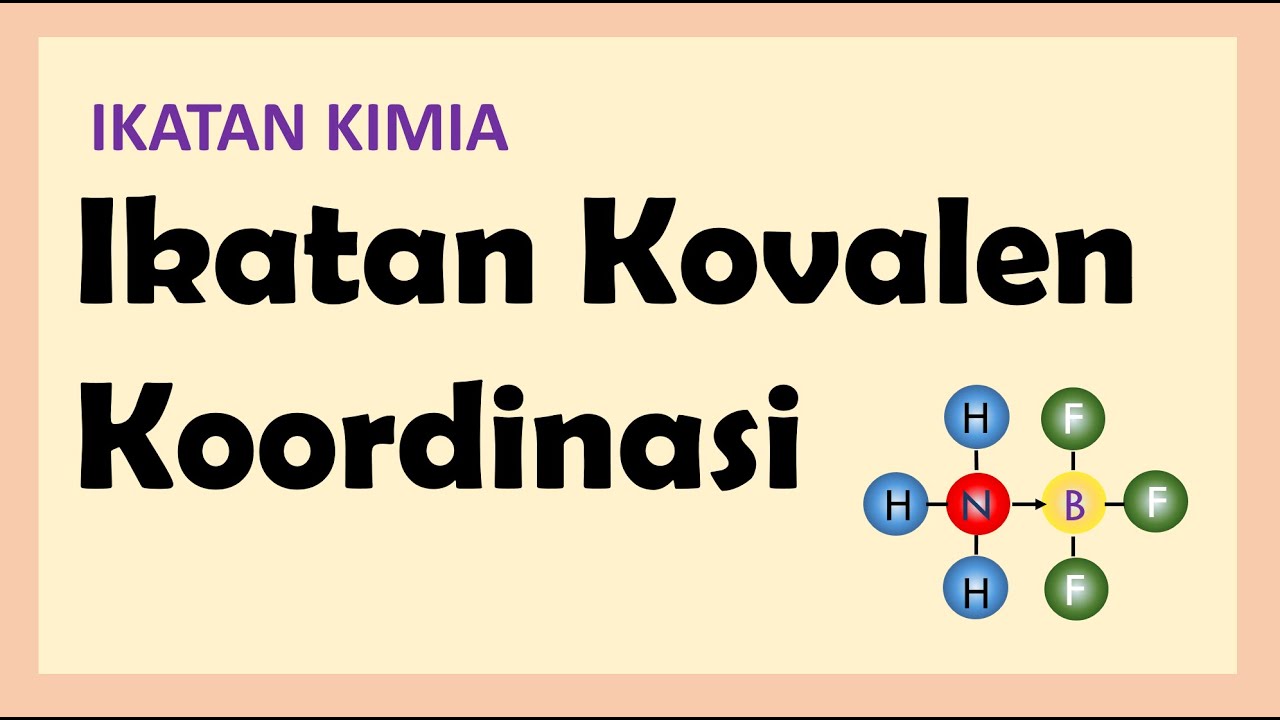
pengertian senyawa ion dan senyawa kovalen Alison Kerr
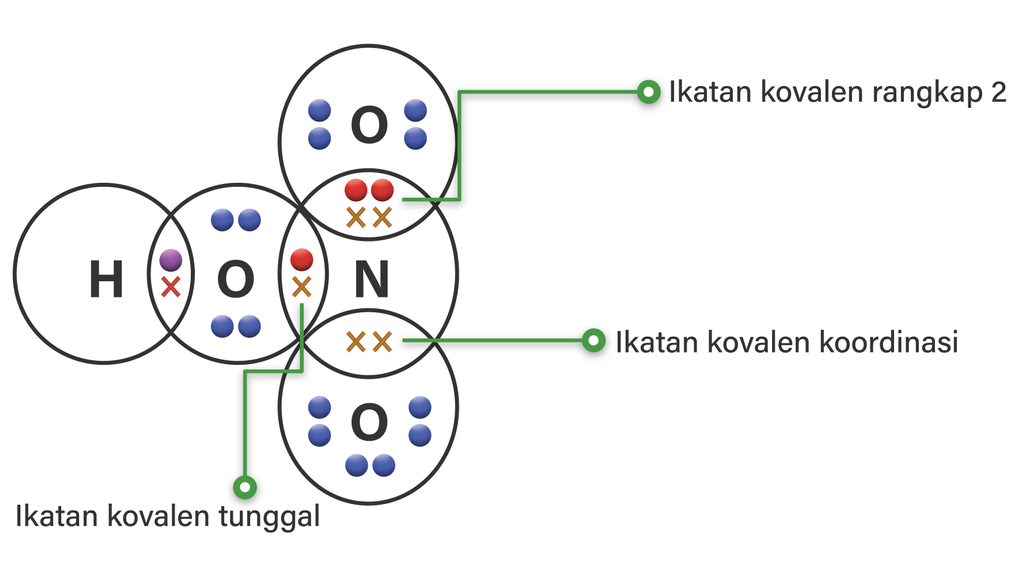
SO3; HNO3. Contoh senyawa dengan ikatan kovalen koordinasi adalah HNO3 atau yang lebih dikenal sebagai asam nitrat. Dalam molekul HNO3 terdapat 3 ikatan kovalen dan 1 ikatan kovalen koordinasi. Baca juga: Jenis-Jenis Ikatan Kimia. NH4Cl. Senyawa NH4Cl terbentuk dari ion NH4+ dan ion Cl-. Ion NH4+ terbentuk dari molekul NH3 dan ion H+.

Tata Nama Senyawa Hidrokarbon Beserta Contoh Soal Dan Pembahasannya My XXX Hot Girl
Tunjukkan ikatan kovalen koordinasi pada senyawa: a. SO3 b. HNO3 c. NO2. Ikatan Ion dan Ikatan Kovalen; Ikatan Kimia, Bentuk Molekul, dan Interaksi Antarmolekul. Tentukan atom pusatnya namun pada senyawa ini terdapat aturan yaitu atom H harus berikatan langsung dengan oksigen atau atom O ini berlaku untuk semua asam oksi maka penempatannya.

Gugus fungsi yang terdapat dalam senyawa organik berikut
Pada senyawa SO3, terdapat ikatan kovalen polar yang menghubungkan satu atom unsur belerang dengan tiga atom unsur oksigen. Ikatan ini terbentuk melalui pertukaran pasangan elektron, di mana belerang memberikan dua elektron sementara oksigen masing-masing memberikan satu elektron. Penjelasan lebih lengkap mengenai ikatan tersebut dapat membantu memahami sifat dan karakteristik senyawa SO3.

Gambarkan Struktur Lewis Untuk Senyawa Na2O bukubelajarstate
Pada senyawa SO3, terdapat ikatan kovalen polar antara atom belerang dan tiga atom oksigen. Keberadaan ikatan rangkap tiga membuat senyawa ini sangat reaktif dan bersifat korosif. SO3 digunakan dalam berbagai industri, seperti produksi asam sulfat, pembuatan surfaktan, dan sebagai katalisator. Namun, penanganan SO3 harus dilakukan dengan hati.

Pada senyawa SO3 terdapat ikatan
Ikatan kovalen cenderung terjadi pada atom nonlogam. Molekul SO2 terbentuk melalui ikatan kovalen. Hal ini dikarenakan S dan O merupakan unsur nonlogam. Pada molekul SO2 terdapat empat ikatan kovalen, dimana 1 atom S berikatan dengan 2 atom O. Pada setiap ikatan, atom O dan S saling menyumbangkan 2 elektron untuk dijadikan milik bersama.

3 contoh senyawa ion kovalen dan logam Alexandra Springer
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Ikatan ion terdapat pada.
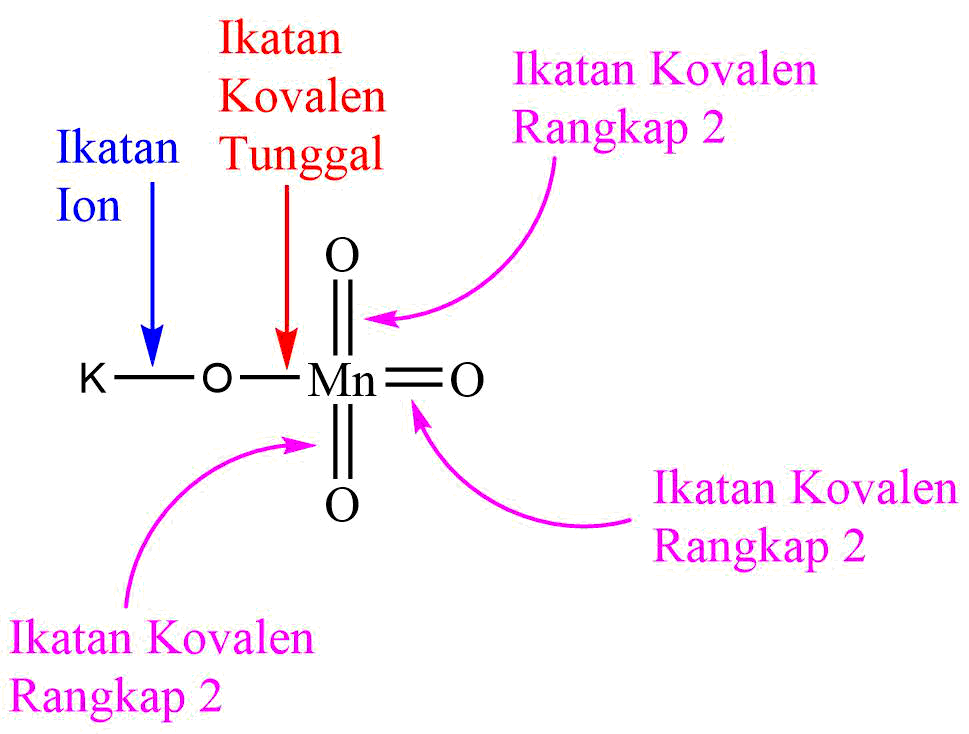
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
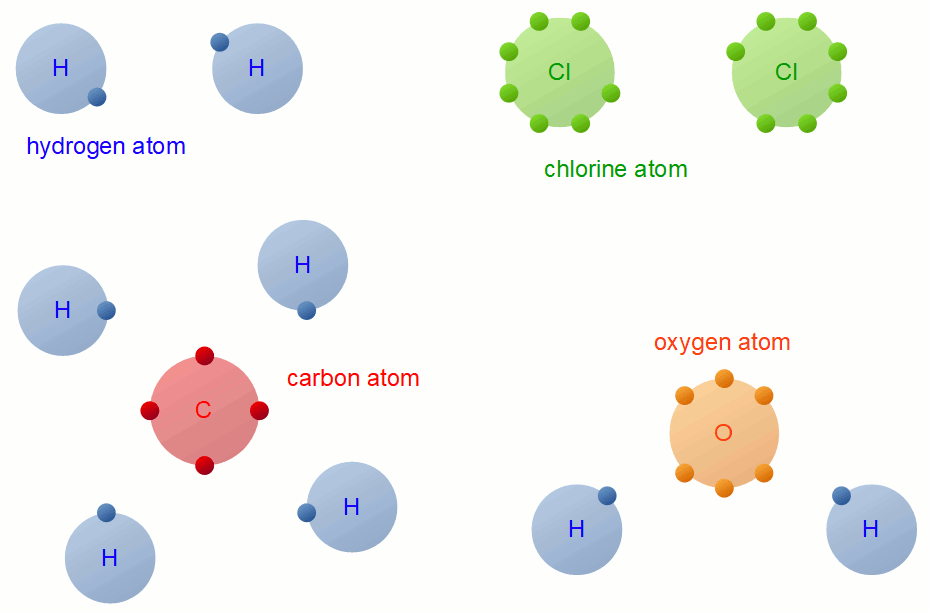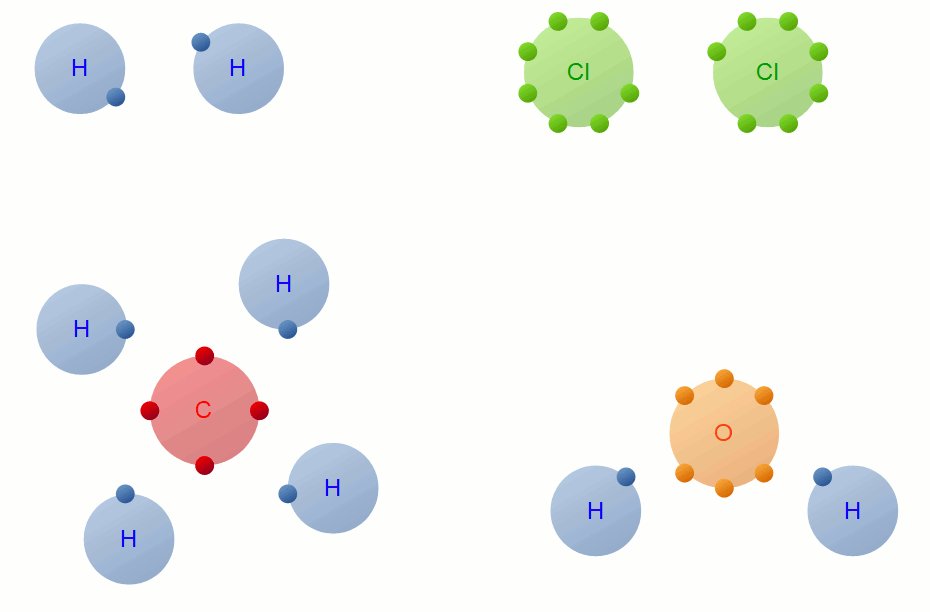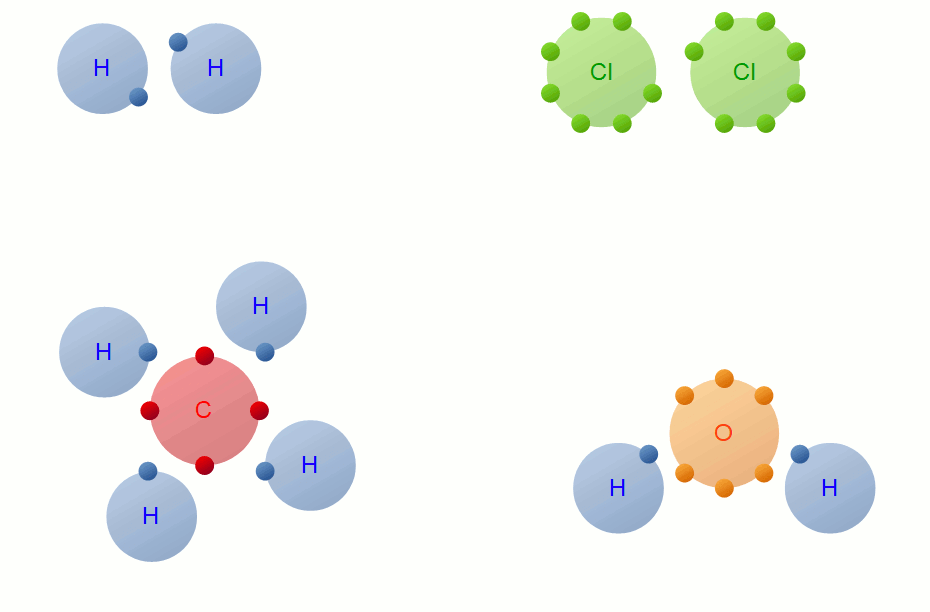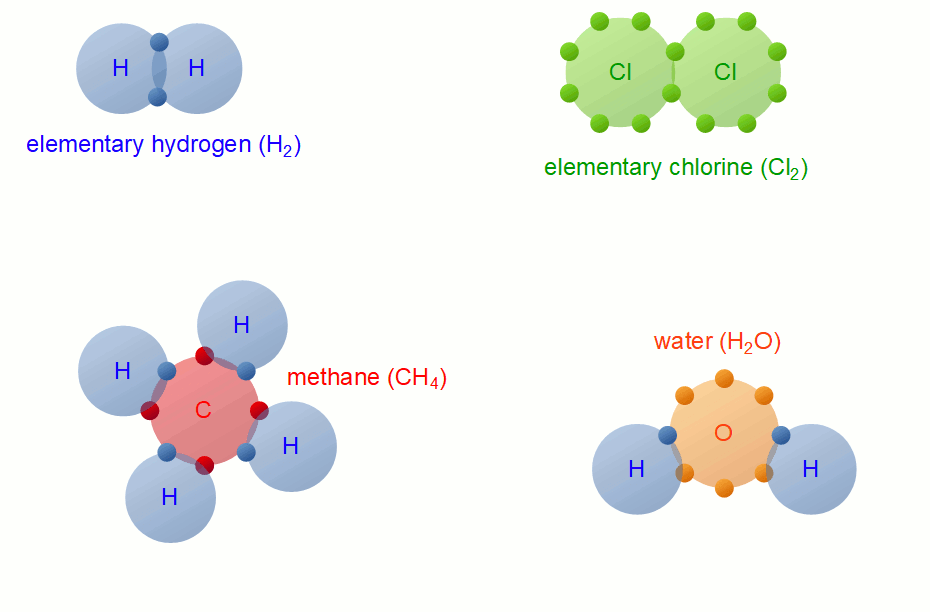
Contoh ikatan kovalen jenis ini adalah pembentukan senyawa HCl dan CH4. a. Pembentukan HCl. Konfigurasi elektron 1H : 1s1 sehingga elektron valensinya = 1. Untuk mencapai konfigurasi elektron yang stabil (sesuai kaidah duplet) diperlukan 1 elektron. Konfiguarsi elektron 17Cl adalah 1s2 2s2 2p6 3s2 3p5 sehingga CI dan mempunyai elektron valensi = 7.
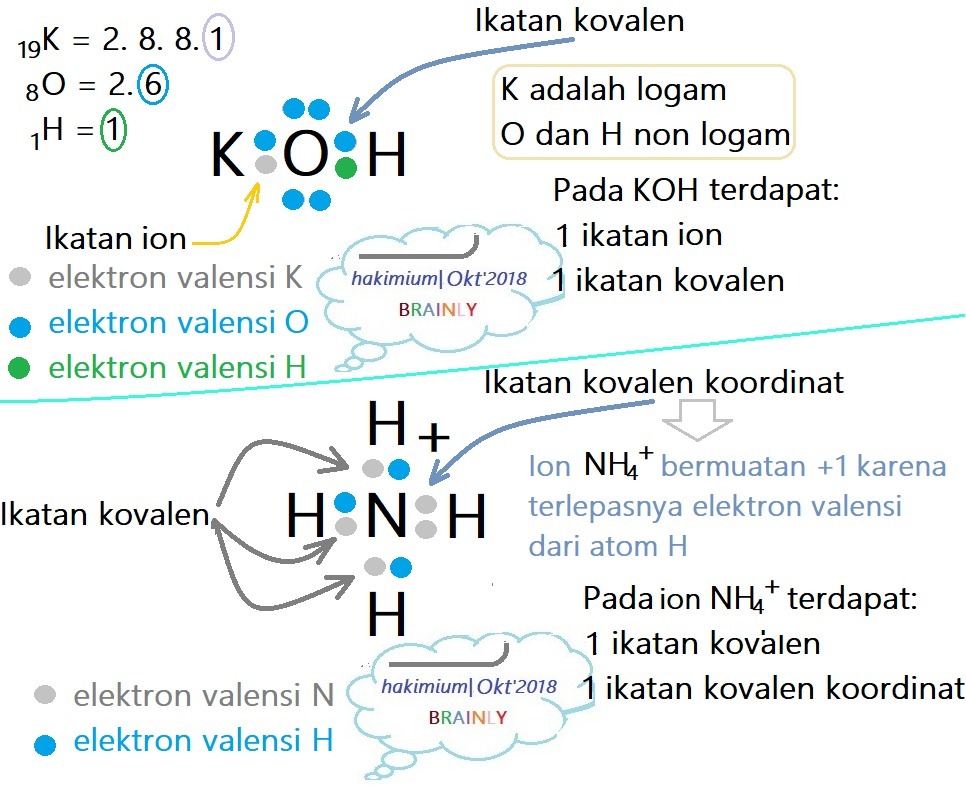
Pembahasan Soal Senyawa dan Ion yang Mempunyai Ikatan Kovalen dan Ikatan Ion Sekaligus MateriKimia
Kalau ikatan kovalen nonpolar, pasangan elektron ikatannya akan sama kuat ke semua atom, di mana keelektronegatifan antar ikatannya sama. Contohnya adalah atom H yang berikatan dengan atom H lagi, keduanya memiliki nilai keelektronegatifan masing-masing 2,1. Contoh lainnya adalah minyak. Nah, itu dia jenis-jenis ikatan kovalen.

Gambarkan ikatan kovalen dalam senyawa yang terbentuk pad...
Pada unsur O, subkulit p juga tidak terisi penuh sehingga membutuhkan 2 elektron untuk dapat stabil memenuhi orbital subkulit p. Pada pengisian elektron di subkulit 2p4 terlihat hanya satu pasang elektron yang berpasangan dan 2 pasang elektron bebas. Satu unsur S kemudian akan berikatan dengan 3 unsur O membentuk senyawa SO3:
contoh senyawa ion dan kovalen dalam kehidupan sehari hari Samantha Hemmings
Untuk lebih jelasnya, yuk simak pembahasan berikut ^_^ Senyawa SO3 terdiri dari atom S dan atom O. Sebelum menentukan jenis ikatan pada senyawa tersebut, sebaiknya kita perlu mengetahui konfigurasi elektron dari masing-masing atomnya. S = 1s2 2s2 2p6 3s2 3p4 (elektron valensi = 6 yaitu 3s2 3p4) O = 1s2 2s2 2p4 (elektron valensi = 6 yaitu 2s2.

Tata Nama Senyawa Kimia, Berikut Ini Penjelasannya untuk Anda
Jadi,ikatan pada senyawa NaF merupakan ikatan Ionik ya. Terjadi perpindahan elektron valensi Na ke F untuk membentuk senyawa yang stabil (sumber gambar: wikipedia) Ikatan ionik hanya dapat terjadi antar unsur-unsur yang memiliki perbedaan keelektronegatifan cukup besar. Sehingga, terjadi serah terima elektron seperti pada contoh di atas.

Detail Contoh Senyawa Ikatan Kovalen Koleksi Nomer 7
SO3 merupakan rumus kimia yang mewakili senyawa Serangan Oksigen Trioksida. Senyawa ini terdiri dari satu atom sulfur (S) dan tiga atom oksigen (O). Dalam keadaan normal, SO3 berbentuk gas tipis berwarna putih, tidak berbau. Namun, pada suhu rendah, SO3 dapat berubah menjadi padatan yang keras dan tidak berwarna. Sifat-sifat SO3

Cara Identifikasi Keberadaan Ikatan Kovalen Koordinasi pada Suatu Molekul Serba Ada
Soal 23. Pada senyawa SO3 terdapat ikatan . . . a. Ikatan ion b. Ikatan hidrogen c. Ikatan kovalen dan Ikatan kovalen koordinasi d. Ikatan ion dan logam e. Ikatan kovalen dan ion. Jawaban: C. Pembahasan: Ikatan kovalen koordinasi terjadi jika pada pembentukkan ikatan terdapat pasangan elektron yang hanya berasal dari salah satu atom yang.

Diantara kelompok senyawa berikut yang kesemuanya terdapat ikatan kovalen koordinasi adalah
Baca baik-baik ya! —. 1. Pengertian. Ikatan ion terjadi akibat adanya serah terima elektron sehingga membentuk ion positif dan ion negatif yang konfigurasi elektronnya sama dengan gas mulia. Ion positif dan ion negatif diikat oleh suatu gaya elektrostatik. Senyawa yang dihasilkan disebut senyawa ion.
Pada senyawa terdapat ikatan IlmuanTekno
Pada senyawa SO3 terdapat ikatan. Ikatan Ion dan Ikatan Kovalen; Ikatan Kimia, Bentuk Molekul, dan Interaksi Antarmolekul. Pertanyaan lainnya untuk Ikatan Ion dan Ikatan Kovalen. Perhatikan data sifat fisik dari dua buah zat berikut.. Tonton video. Tabel berikut menunjukkan sifat-sifat senyawa Q dan R.se. Tonton video. Unsur 17R dan.

Ikatan apa saja yang terdapat pada senyawa KClO3 ? Brainly.co.id
Struktur dan ikatan. SO 3 dalam bentuk gas merupakan molekul trigonal planar dengan simetri D 3h, sebagaimana yang diprediksi pada teori VSEPR.SO 3 berada dalam point group D 3h.. Dalam hal perhitungan muatan formal, atom belerang memiliki bilangan oksidasi +6 dan muatan formal +2. Struktur lewis senyawa ini terdiri dari sebuah ikatan rangkap dua S=O dan dua ikatan datif S-O tanpa.