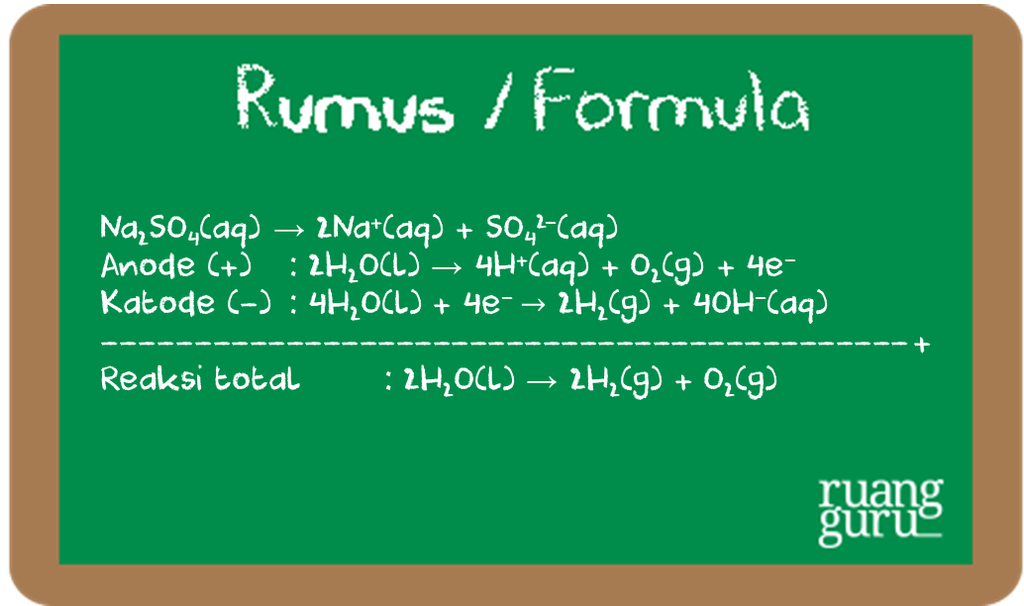
ReaksiReaksi pada Sel Elektrolisis Kimia Kelas 12 Belajar Gratis di Rumah Kapan Pun! Blog
electrolysis, process by which electric current is passed through a substance to effect a chemical change. The chemical change is one in which the substance loses or gains an electron (oxidation or reduction). The process is carried out in an electrolytic cell, an apparatus consisting of positive and negative electrodes held apart and dipped.
Contoh Soal Dan Pembahasan Elektrolisis Soal Kelasmu
Arus listrik akan dialirkan melalui larutan H2SO4 dan Co akan mengendap pada katoda dalam bentuk logam Co. Intensitas arus dan waktu elektrolisis akan mempengaruhi sejauh mana proses pemisahan Co dapat berjalan. Jadi, dengan melakukan elektrolisis pada larutan H2SO4 yang mengandung Co, Anda dapat menghasilkan logam Co yang murni.
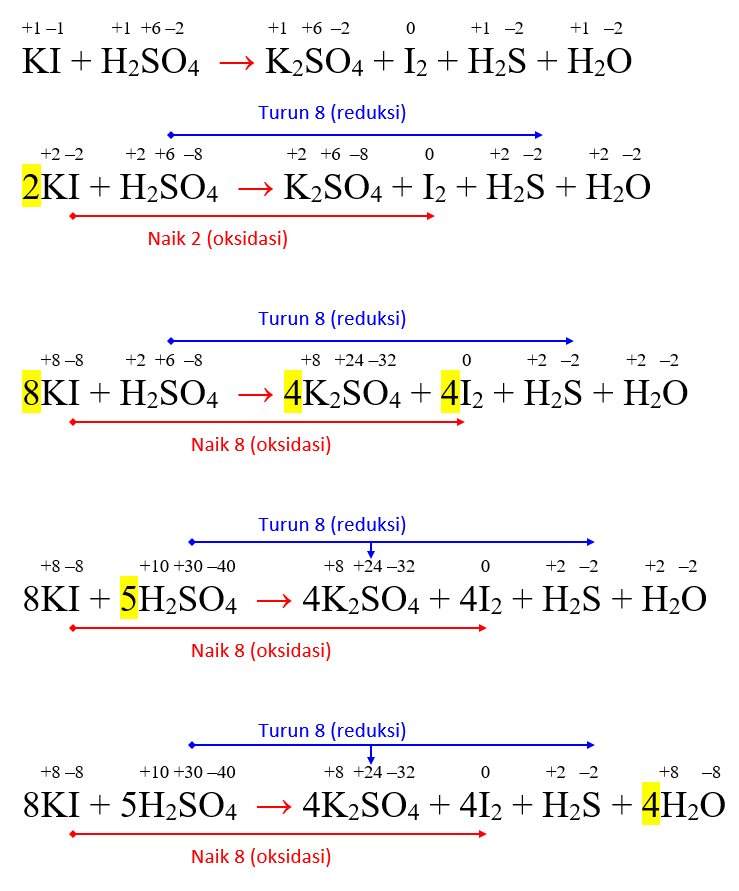
Penyetaraan Reaksi Redoks KI + H2SO4 → K2SO4 + I2 + H2S + H2O Serba Ada
In some textbooks, it may be said that for the electrolysis of dilute H2SO4 H 2 S O 4, the oxidation half-equation is written as 2HX+ +2eX− HX2 2 H X + + 2 e X − H X 2 and the reduction half-equation is written as 4OHX− 2HX2O +OX2 +4eX− 4 O H X − 2 H X 2 O + O X 2 + 4 e X −. However, the concentrations of these ions in solution are.
Chemistry ELEKTROLISIS
Dalam 1 mol H2SO4 terdapat 98 gram H2SO4. Jadi, jumlah mol H2SO4 dalam 500 gram larutan adalah: Jumlah mol = (500 g) / (98 g/mol) = 5.102 mol H2SO4. Menggunakan persamaan reaksi elektrolisis 2H2SO4 → 2H2 + O2, kita dapat mengetahui bahwa setiap 2 mol H2SO4 akan menghasilkan 2 mol H2 gas.

MUATAN FORMAL3 MENENTUKAN KESTABILAN STRUKTUR LEWIS H2SO4 YouTube
Saksikan proses seru elektrolisis larutan H2SO4 yang encer menggunakan elektroda PT! Temukan bagaimana reaksi kimia dan perubahan warna yang terjadi dalam percobaan menarik ini. Dapatkan penjelasan lengkap mengenai elektrolisis dan manfaatnya dalam dunia industri serta tips praktisnya. Jangan lewatkan kesempatan untuk mengeksplorasi lebih lanjut mengenai aplikasi elektrolisis dan peranan.
10.Electrolysis of dilute H2SO4 liberates gases at anode and cathode respectively provide me
Jelajahi lautan kimia dengan elektrolisis larutan H2SO4 menggunakan elektroda Pt! Temukan bagaimana reaksi aneh membentuk elemen baru dalam percobaan menegangkan ini. Dapatkan penjelasan mendalam tentang proses elektrolisis dan manfaatnya dalam dunia ilmu pengetahuan. Nikmati perjalanan yang menggairahkan dengan kata kunci: elektrolisis, larutan H2SO4, elektroda Pt, kimia, dan eksperimen.

Pada Elektrolisis Larutan Pbcl2 Menggunakan Elektroda Inert Lengkap
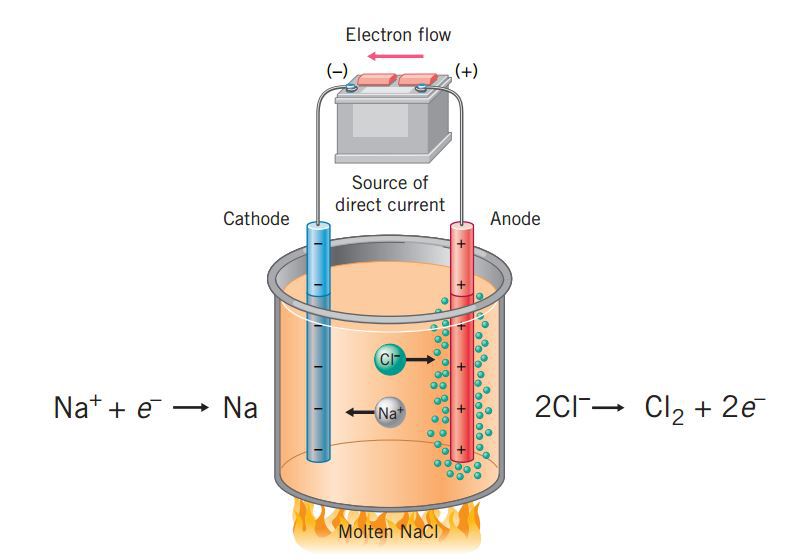
The power supply (battery) must supply a minimum of 4 V, but, in practice, the applied voltages are typically higher because of inefficiencies in the process itself. Figure 17.7.1 17.7. 1: Passing an electric current through molten sodium chloride decomposes the material into sodium metal and chlorine gas.

Zatzat di bawah ini dielektrolisis dengan elektro...
Hasil elektrolisis larutan H2SO4 dengan elektrode Pt dapat digunakan dalam berbagai aplikasi industri, seperti produksi bahan kimia, pemurnian logam, dan sistem penyimpanan energi. Selain itu, hasil elektrolisis ini juga dapat digunakan dalam penelitian dan percobaan di laboratorium untuk mempelajari reaksi redoks. 5.

H2so4 Enthalpy Of Formation
The half-equations for the electrolysis of water (electrolyte of acidified with dilute sulphuric acid). (a) The negative cathode electrode reaction for the electrolysis of water. The negative cathode electrode reaction is a reduction (electron gain). The hydrogen ions (H+) are attracted to the negative cathode and are discharged as hydrogen gas.

Contoh Soal Elektrolisis Homecare24
Pertanyaan. Elektrolisis larutan H2SO4 encer dengan elektroda Pt, dihasilkan 22.4 liter gas hydrogen (diukur pada STP). Jika muatan listrik yang digunakan untuk elektrolisis larutan H2SO4 tersebut dalam jumlah sama digunakan untuk elektrolisis larutan CuSO4, massa tembaga yang diendapkan adalah..
Electrolysis of H2SO4 (conc.) gives the following atanode (1) H2 (2) O2 (3) H2S203 (4) H2S2O8
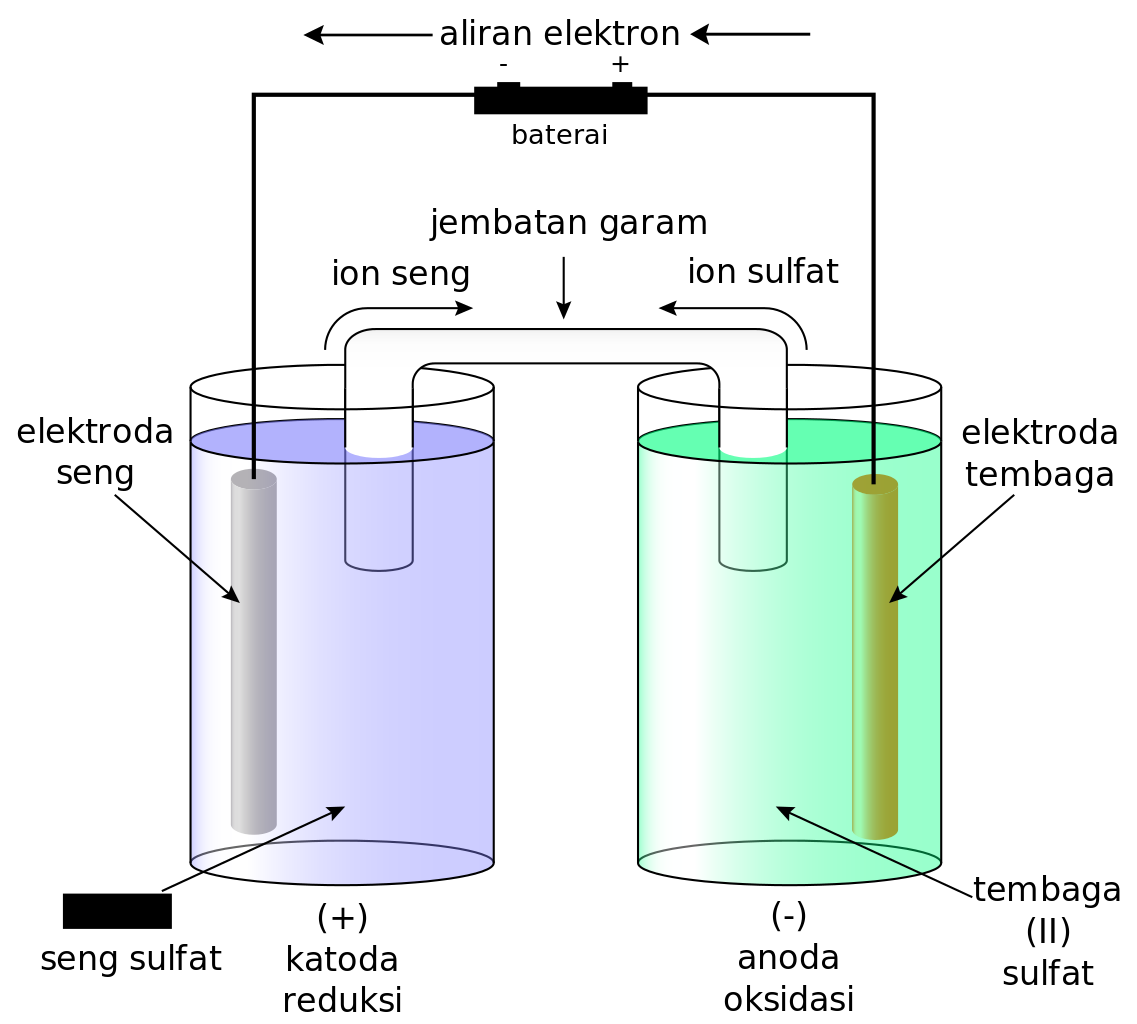
Secara teoritis, sel elektrolisis merupakan bagian dari sel elektrokimia, di mana energi listrik digunakan untuk menjalankan reaksi redoks tidak spontan. Secara umum, sel elektrolisis tersusun dari: - Elektrolit, yaitu zat yang dapat menghantarkan listrik. - Sumber listrik yang menyuplai arus searah ( Direct Current = DC), misalnya baterai.

Pada elektrolisis larutan CuSO4 seperti terlihat pada gam...
This video shows the operation of an electrolytic cell & the experimental method of electrolysis. It carefully visualizes the mechanism of electrolysis in wh.

37+ Materi Dan Contoh Soal Elektrolisis Rochelle Proctor
jadi, ini soal dan jawaban mengenai reaksi elektrolisis larutan H2SO4 menggunakan elektroda grafit. kebetulan di sekolahku ada soal seperti ini.maaf jika ban.

Aktiviti Makmal 1F Kimia Tingkatan 5 Elektrolisis Larutan CuSO4 dan H2SO4 cair YouTube
During an electrolysis of conc. H2SO4, perdisulphuric acid (H2S2O8) and O2 form in equimolar amount. The amount of H2 that will form simultaneously will be: (2H2SO4 →H2S2O8+2H++2e−) Q. During the electrolysis of conc H2SO4, it was found that H2S2O8 and O2 were liberated in a molar ratio of 3:1.
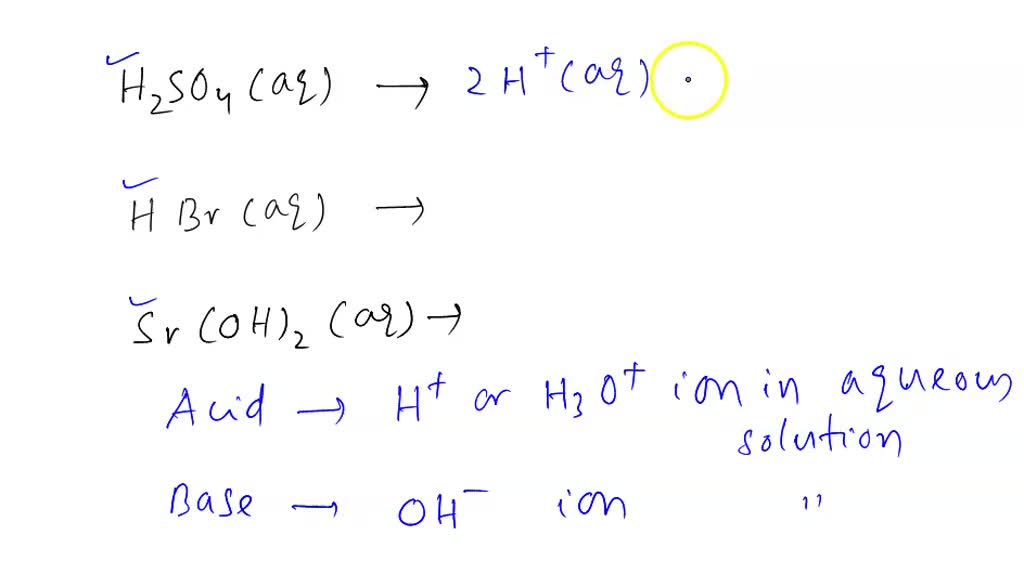
SOLVED Show the two step dissociation process for H2SO4. Do both acidic hydrogens dissociate 100?
tuliskan reaksi elektrolisis larutan H2SO4 dengan. AU. ALDHA U. 26 Oktober 2021 02:20. Pertanyaan. tuliskan reaksi elektrolisis larutan H2SO4 dengan elektroda C 57. 1. Jawaban terverifikasi. Iklan. Iklan. ML. M. Larasati. 27 Oktober 2021 21:21. Jawaban terverifikasi. Hai Adha, Kakak coba bantu jawab. Elektrolisis ialah mengubah energi.
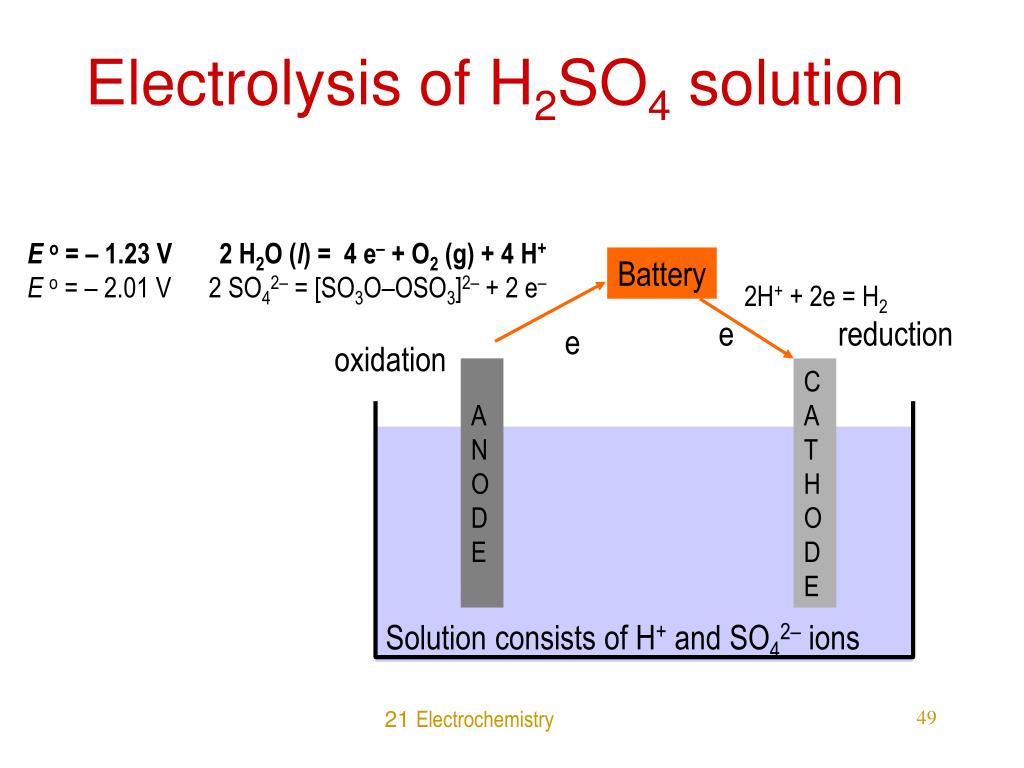
PPT 21 Electrochemistry PowerPoint Presentation, free download ID826545
Pada elektrolisis larutan garam logam alkali dan alkali tanah tidak terbentuk logamnya, tetapi terbentuk gas H 2 . Hal ini disebabkan E o reduksi ion logam alkali dan alkali tanah.. 17. 0.0. Jawaban terverifikasi. Iklan. Iklan. Larutan Na 2 SO 4 dielektrolisis dengan elektroda Pt. Zat yang dihasilkan di katoda adalah.