
Sifat Koligatif Larutan Part 1 Penurunan Tekanan Uap dan Kenaikan Titik Didih YouTube
Laporan Kenaikan Titik Didih Larutan 6, April 2013 BAB I PENDAHULUAN I. Judul Kenaikan titik didih larutan II. Latar Belakang Titik didih adalah suhu dimana cairan mendidih, dimana tekanan uap sebuah zat cair sama dengan tekanan eksternal yang dialami cairan. Larutan dapat dibagi menjadi dua berdasarkan nilai titik didih zat terlarut. Pertama.

SIFAT KOLIGATIF LARUTAN KENAIKAN TITIK DIDIH YouTube
Sifat koligatif larutan adalah sifat larutan yang tidak bergantung pada jenis dan ukuran zat terlarut, tetapi hanya bergantung pada jumlah partikel zat terlarut. Sifat koligatif larutan meliputi : Penurunan tekanan uap (∆P) Kenaikan titik didih (∆Tb) Penurunan titik beku (∆Tf) Tekanan osmotik (π) 2.3. Penurunan Tekanan Uap.
Kenaikan Titik Didih Dan Penurunan Titik Beku Riset
Jumlah partikel terlarut sebenarnya sebanding dengan berat jenis dari larutan maka akan terjadi hubungan, jika berat jenis bertambah maka titik beku dan kenaikan titik didih dari pelarut murninya akan menurun (Sitanggang, 2019). Titik didih adalah suhu pada saat tekanan uap cari sama dengan tekanan di permukaan.

KENAIKAN TITIK DIDIH ELEKTROLITNONELEKTROLIT YouTube
Sehingga akan dapat menambah pemahaman mengenai kenaikan titik didih zat. iv f BAB II KAJIAN TEORI A. Kenaikan Titik didih Suhu dimana cairan mendidih dinamakan titik didih. Jadi, titik didih adalah temperatur dimana tekanan uap sama dengan tekanan atmosfer. Selama gelembung terbentuk dalam cairan, berarti selama cairan mendidih, tekanan uap.

Kenaikan Titik Didih PDF
dalam mencapai titik didih semakin cepat sebesar koefisien nilai b. Adapun data yang dimaksud adalah sebagai berikut : a. Rumus uji t untuk koefisien korelasi parsial konsentrasi larutan terhadap waktu titik didih larutan : 𝑡 = 𝑟𝑝√ − √1−𝑟𝑝2 (Hasan, 2004) 3 b. regresi linier untuk konsentrasi larutan

Sifat Koligatif Larutan Part 2 Kenaikan Titik Didih dan Penurunan Titik Beku Kimia Kelas XII
Membandingkan kenaikan titik didih larutan nonelektrolit dan larutanelektrolit pada konsentrasi yang sama. III. Landasan Teori : Suhu dimana cairan mendidih dinamakan titik didih. Jadi, titik didih adalah temperatur dimana tekanan uap sama dengan tekanan atmosfer.. Kimia Dasar II Organik (FPU6171) 54 Documents. Students shared 54 documents.

KIMIA KELAS XII SIFAT KOLIGATIF LARUTAN "KENAIKAN TITIK DIDIH LARUTAN" YouTube
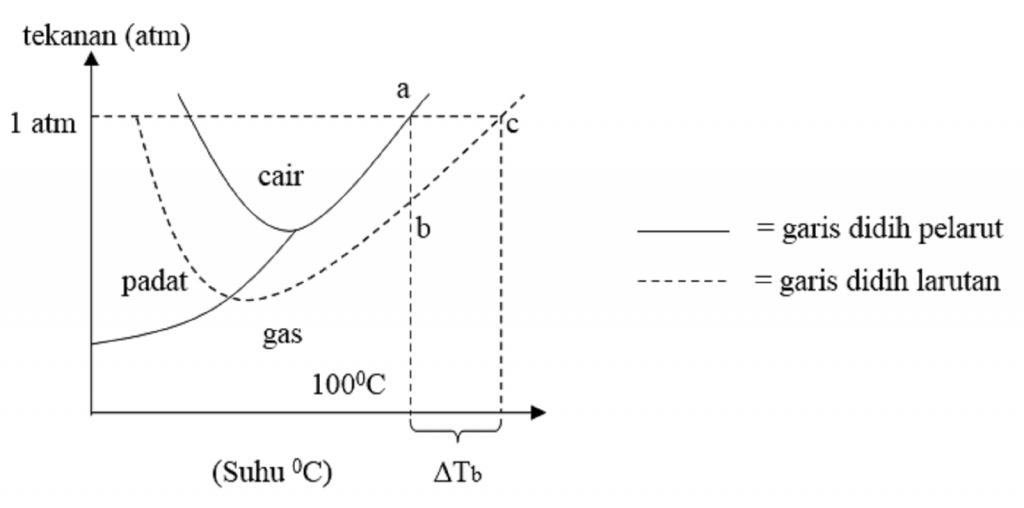
Selisih antara titik didih larutan dengan titik didih pelarut inilah yang disebut dengan kenaikan titik didih ( ∆T b ). Rumus untuk menentukan kenaikan titik didih ( ∆T b ) adalah: Untuk larutan yang bersifat elektrolit, maka persamaannya akan berubah menjadi: T b = K b . m [ 1 + ( n - 1 ) α ]
Kenaikan Titik Didih Penurunan Titik Beku Sifat Koligatif Larutan Reverasite
Titik didih alkana dalam deret homolognya mengalami kenaikan sebesar kurang lebib 30 0C untuk setiap penambahan CH 2. Akan tetapi, adanya percabangan dalam struktur molekul hidrokarbon cenderung menurunkan titik didih. Umumnya, kenaikan titik didih disebabkan meningkatnya gaya tarik Van Der Waals antara molekul.
Cara Menentukan atau Menghitung Kenaikan Titik Didih Larutan SERBA SERBI
Kenaikan titik didih. Kenaikan titik didih menggambarkan fenomena bahwa titik didih dari cairan (suatu pelarut) akan lebih tinggi ketika senyawa lain ditambahkan, yang berarti bahwa larutan akan memiliki titik didih yang lebih tinggi daripada pelarut murninya. Hal ini terjadi ketika zat terlarut yang tidak mudah menguap, seperti garam.

Contoh Soal Kenaikan Titik Didih Larutan (Sifat Koligatif Larutan Elektrolit) YouTube
Tujuan : 1. Menyelidiki titik didih larutan serta faktor yang mempengaruhi. 2. Membandingkan kenaikan titik didih larutan nonelektrolit dan larutanelektrolit pada konsentrasi yang sama. III. Landasan Teori : Suhu dimana cairan mendidih dinamakan titik didih. Jadi, titik didih adalah temperatur dimana tekanan uap sama dengan tekanan atmosfer.

Bab iv kenaikan titik didih
Persiapan UTBK 2023 Lengkap di aplikasi Pahamify: https://linktr.ee/mipipahamifyBersama Kak Yuli, kita akan belajar tentang 2 sifat koligatif larutan, kenaik.

Melihat Proses Kenaikan Titik Didih Kimia Kelas 12 Belajar Gratis di Rumah Kapan Pun! Blog
LAPORAN PRAKTIKUM Kenaikan titik didih. devi nadiya widjaya. Download Free PDF View PDF. Laporan titik leleh dan titik didih. Devii Purba.. Menentukan titik didih beberapa zat II. DASAR TEORI A. TITIK LELEH Titik leleh adalah temperatur dimana zat padat berubah wujud menjadi zat cair pada tekanan satu atmosfer. Dengan kata lain, titik leleh.

Tetapan kenaikan titik didih molal (Kb) tergantung pada.
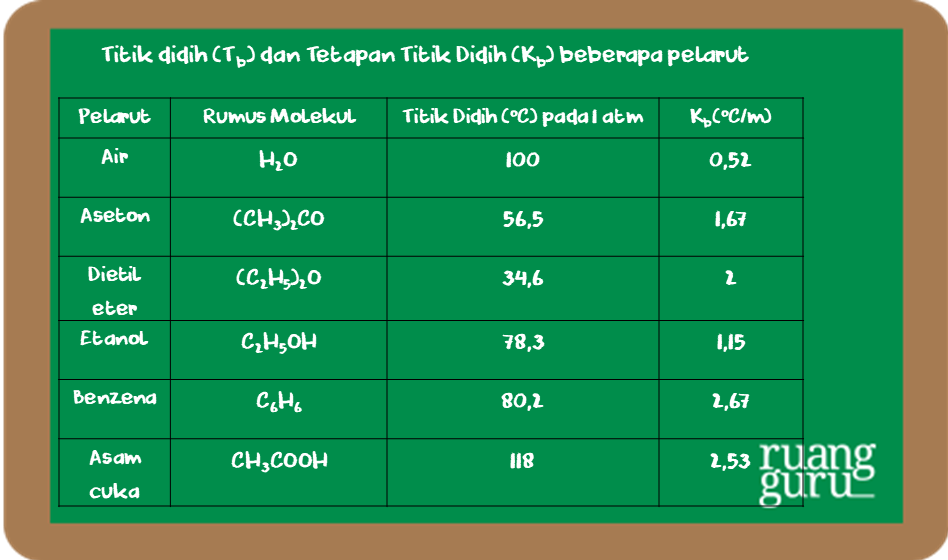
Persamaan yang digunakan adalah: ∆Tb = Tb (larutan) - Tb (pelarut) ∆Tb = m . Kb. Dengan, ∆ Tb =kenaikan titik didih (boiling point elevation) m = molalitas. Kb = tetapan kenaikan titik didih (oC kg/mol) Titik didih melibatkan lebih dari satu fase kondisi atau fase zat terkait (fase cair-gas).
Melihat Proses Kenaikan Titik Didih Kimia Kelas 12
T b° = titik didih pelarut murni (air) T b = titik didih larutan. Kenaikan titik didih hanya tergantung pada jenis pelarut dan molaritas larutan, tidak tergantung pada jenis zat terlarut. Jika ditambahkan zat terlarut yang tidak mudah menguap, misalnya gula, maka dibutuhkan kenaikan titik didih yang cukup besar agar dapat mendidih.

Soal Kenaikan Titik Didih Dan Penurunan Titik Beku Reverasite
Jumlah partikel terlarut sebenarnya sebanding dengan berat jenis dari larutan maka akan terjadi hubungan, jika berat jenis bertambah maka titik beku dan kenaikan titik didih dari pelarut murninya akan menurun (Sitanggang, 2019). Titik didih adalah suhu pada saat tekanan uap cari sama dengan tekanan di permukaan.

kenaikan titik didih(penjelasan di deskripsi) YouTube
Tb = 100°C + ΔTb. = 100°C + 0,0416°C = 100,0416°C. Jadi, Tidik didih larutan tersebut yaitu 100,0416°C. Itulah ulasan mengenai √ Titik Didih : Pengertian, Kenaikan, Faktor, Rumus & Contoh Soalnya Lengkap. Semoga apa yang telah diulas dapat bermanfaat bagi pembaca. Sekian dan terima kasih.