
suatu larutan mengandung 425 gram H2SO4. berat jenis larutan 1.2875 g
1. Hitung kemolaran glukosa, jika 17,1 gram sukrosa (C 12 H 22 O 11) dilarutkan dalam air sehingga volume larutan mejadi 500 ml. Pembahasan Diketahui: Massa sukrosa = 17,1 Mr C 12 H 22 O 11 = 342 volume = 500 ml = 0,5 l Ditanya: Kemolaran (M)…? Jawab: n = gram/Mr n = 17,1/342 n = 0,05 mol Kemolaran (M) = n/v M = n/v M = 0,05/0,5 M = 0,1 M 2.

Kemolalan Suatu Larutan 10 Massa Urea Mr 60 Adalah sisi tegak pada
Soal dan Jawaban Konsentrasi Larutan: Molaritas, Molalitas, Fraksi Mol, Persen Berat, Normalitas. 1. Konversi molal ke % massa. Contoh soal: Hitunglah % massa dari larutan NaI 0,2 molal (massa molar NaI = 150 g/mol) Penyelesaian: Arti 0,2 molal NaI adalah 0,2 mol NaI dalam 1 Kg pelarut air. massa NaI sebanyak 0,2 mol = 0,2 mol x 150 g/mol = 30 g.

Kimia Perbedaan mol,molaritas dan kemolalan YouTube
Kemolalan ( m) merupakan perbandingan antara jumlah mol zat terlarut dengan massa (kg) zat pelarut. Secara matematik dapat di rumuskan sebagai berikut : Keterangan : m = molalitas n = mol zat terlarut p = massa za pelarut (gram)

CARA MENGHITUNG KEMOLALAN JIKA DIKETAHUI PERSEN MASSA ZAT TERLARUTNYA
Rumus fraksi mol zat pelarut. Zat pelarut adalah suatu zat yang dapat melarutkan bahan lain dan membentuk campuran atau larutan. Biasanya, zat pelarut merupakan zat cair baik yang bersifat polar maupun non polar. Rumus fraksi mol zat pelarut adalah: Dengan, xp: fraksi mol zat pelarut. np: jumlah mol zat pelarut.

Rumus Torsi/ Momen Gaya (2)
Rumus kemolaran adalah:kemolaran = massa zat terlarut (g) / volume larutan (L) x massa molar zat terlarut (g/mol)Contohnya, jika kita memiliki 90 gram gula dalam 1 liter air dan massa molar gula adalah 342,3 g/mol, maka kemolaran gula adalah 0,262 M. Perbedaan Antara Kemolalan dan Kemolaran

Contoh Soal Kemolalan Kelas 12 Pembelajaran Siswa
Asam cuka sebanyak 115 ml dilarutkan di dalam 45 ml air. Hitung % V dari larutan ini. Jawaban. Pengertian dan Contoh Soal Fraksi Mol Lengkap Foto: Screenshoot. 3. Contoh soal fraksi mol berapa gram kalsium hidroksida Ca (OH)² yang terdapat dalam 500 ml larutan 0,2 M Ca (OH)²? (a) 3,7 gram. (b) 7,4 gram. (c) 0,37 gram.

Rumus Bangun Ruang
Kemolalan memuat informasi tentang jumlah zat terlarut dan pelarut sehingga mudah dipakai untuk menghitung fraksi mol, jika kerapatan larutan diketahui. Nilai kemolalan dapat pula digunakan untuk menghitung nilai kemolaran.. Rumus Menentukan Jumlah Massa Zat Ditambahkan Untuk Membuat Normalitas Larutan.

Rumus Menghitung Harga Saham Penutupan My XXX Hot Girl
Secara matematis rumus dari molalitas adalah sebagai berikut. Keterangan: m = molalitas (mol/kg) Mr = massa molar zat terlarut (g/mol) massa = massa zat terlarut (gram) p = massa zat pelarut

Pengertian Fraksi Mol Rumus Dan Contoh Soalnya Materi Kimia Kelas Riset
Home » Matematika » Fraksi Mol Kimia - Xi - Rumus, Penjelasan, Contoh Soal dan Jawaban. Fraksi Mol Kimia - Xi - Rumus, Penjelasan, Contoh Soal dan Jawaban. 07/08/2019 5 min read. Fraksi Mol dalam Kimia. Fraksi mol adalah ukuran konsentrasi larutan yang menyatakan perbandingan jumlah mol sebagian zat terhadap jumlah mol total komponen.

Rumus Molaritas RUANG BACA
100, 0128 ∘ C. 5. 100, 0234 ∘ C. Belajar Modul, Rumus, & Soal Sifat Koligatif Larutan dan kuis interaktif. Dapatkan Modul, Rumus, & Soal Sifat Koligatif Larutan lengkap di Wardaya College.
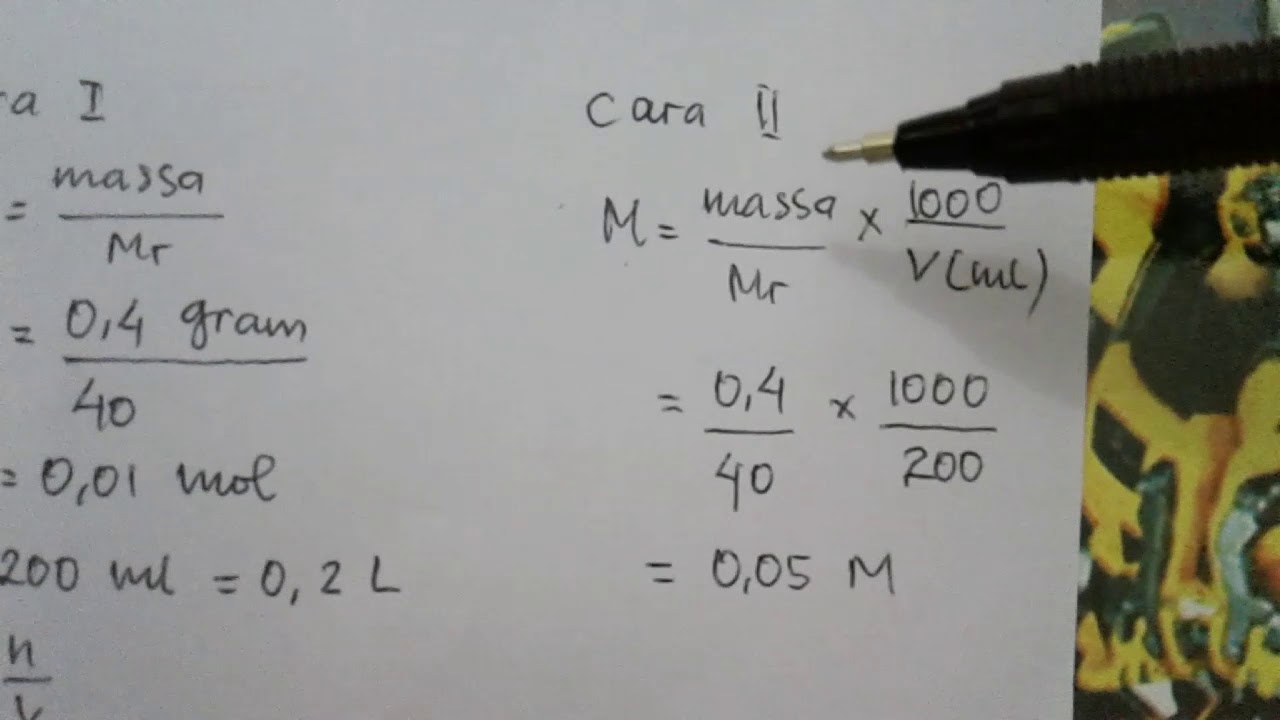
Menghitung Kemolaran ( Stoikiometri) YouTube
1 Rumus Molalitas 1.1 Hubungan Molalitas dengan Persen massa 2 Fraksi Mol 2.1 Fraksi mol zat terlarut (Xt) 2.2 Fraksi mol zat pelarut (Xp) 3 Contoh Soal Molalitas dan Penyelesainya Rumus Molalitas Keterangan m = molalitas (mol/kg) g = gram zat terlarut (g) Mm = massa molar zat (g/mol) P = massa zat pelarut (g) Hubungan Molalitas dengan Persen massa
dio ersa putra Larut dan Pelarut Kimia
Molalitas (M) = jumlah mol zat pelarut / 1 kg zat pelarut. M = g/Mm x 1000/p Dengan keterangan : M = molalitas (mol/kg) g = gram zat terlarut (g) Mm = massa molar zat (g/mol) P = massa zat pelarut (g)

10 Rumus Bangun Datar Luas Keliling Dan Contoh Soal Riset
Banyaknya atom atau partikel yang terdapat dalam 12 gram C-12 adalah 6, 02 × 1023 partikel yang disebut dengan tetapan Avogadro yang dinyatakan dengan simbol L atau NA. Sehingga hubungan jumlah partikel suatu zat (N) dengan mol dapat dinyatakan sebagai berikut: N = L × n = 6, 02 × 1023 × n Massa atom relatif ( Ar)

Kemolalan Suatu Larutan 10 Massa Urea Mr 60 Adalah sisi tegak pada
Jika rumus molekul formalin adalah CH2O, molalitas larutan tersebut sebesar? Suatu larutan diperoleh dengan melarutkan 11,7 gram NaCl ke dalam 800 gr air, hitunglah kemolalan larutan tersebut! Hitung Mr zat terlarut jika 0,224 gram terlarut dalam 17 gram pelarut menghasilkan larutan dengan konsentrasi 0,0161 molal!

Rumus Keliling Dan Luas Lingkaran Beserta Contoh Soalnya
Contoh Soal Molalitas : Fraksi Mol, Rumus dan Penyelesaiannya. Kemolalan atau molalitas adalah konsentrasi larutan yang menyatakan jumlah mol (n) zat terlarut dalam 1 kg atau 1000 gram pelarut. Perbedaan molalitas dan molaritas yaitu jika molalitas adalah kemolalan atau konsentrasi molal (m) menyatakan banyaknya mol zat terlarut dalam 1000.

Kemolaran
Hubungan antara titik beku larutan dan kemolalan ini dapat dituliskan pada rumus berikut ini. Jika dijabarkan, maka rumus hubungan antara titik beku larutan dan kemolalan ini akan terlihat seperti berikut ini. ΔT f = K f x massaMr x 1.000P: Keterangan: massa = massa zat terlarut (gram)