
Konfigurasi Gas Mulia YouTube
A. Istilah dalam Konfigurasi Elektron. 1. Kulit Elektron, Subkulit, dan Orbital. a. Kulit Elektron. Kulit elektron adalah lintasan tertentu yang memiliki tingkat energi tertentu yang ditempati oleh elektron-elektron suatu atom. Elektron pada atom menempati lintasan tertentu yang disebut dengan kulit elektron atau tingkat energi.

Konfigurasi Elektron dan Elektron Valensi
Pengertian Konfigurasi Elektron. Menurut E-book Cerdas Belajar Kimia, konfigurasi elektron merupakan cara penyusunan elektron dalam suatu atom. Konfigurasi elektron dari atom-atom yang berikatan tersebut berubah menyerupai konfigurasi elektron atom-atom gas mulia. Konfigurasi elektron atom-atom gas mulia dikatan stabil, karena elektron valensi.
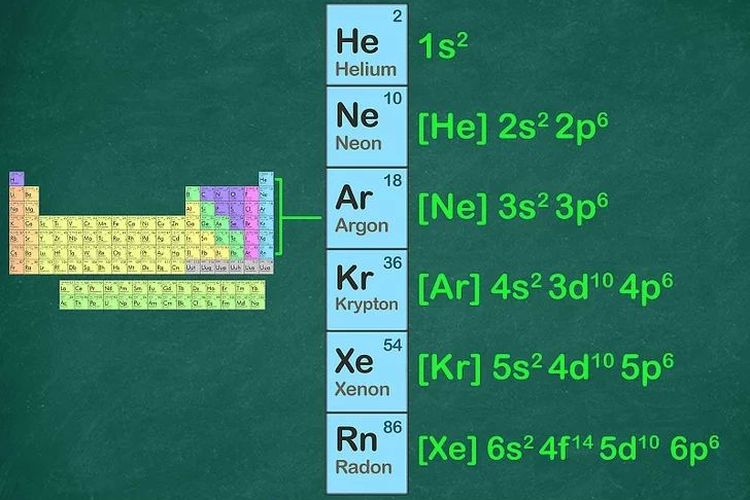
Konfigurasi Elektron Gas Mulia
Pembahasan. Gas mulia adalah unsur yang stabil, karena gas mulia mempunyai konfigurasi elektron valensi yang terisi penuh yaitu, 2 untuk Helium (He) dan 8 untuk Neon (Ne), Argon (Ar), Kripton (Kr), Xenon (Xe) dan Radon (Rn). Berdasarkan hal tersebut maka konfigurasi elektron gas mulia akan memiliki elektron valensi 2 atau 8.
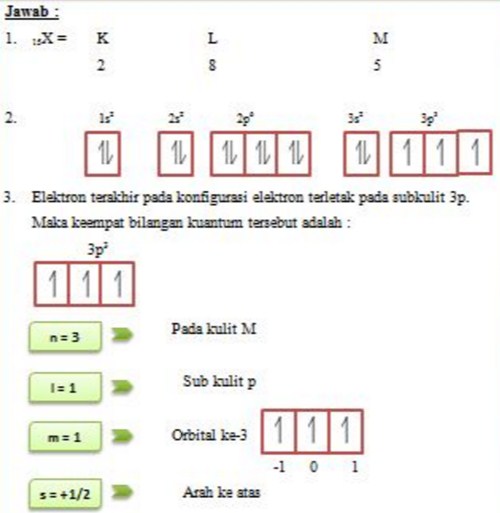
Konfigurasi Elektron Menurut Larangan Pauli Rumus Kimia
Unsur-unsur gas mulia, kecuali radon, dapat ditemukan di udara pada atmosfer meskipun dalam konsentrasi yang sangat kecil. Di antara gas mulia, argon merupakan yang paling banyak terdapat di udara dengan kadar 0,93% dalam udara kering (bebas uap air). Helium lebih banyak ditemukan dalam gas alam (dengan kadar ~1%) daripada dalam udara (~0,00052%).

Memahami Konfigurasi Elektron dan Diagram Orbital Lebih Mudah Kimia Kelas 10
Konfigurasi Elektron Gas Mulia adalah cara untuk menggambarkan atom dalam hal jumlah elektron yang terdapat pada kulit atom. Dalam kimia, konfigurasi elektronik ini merupakan salah satu konsep dasar yang sangat penting untuk dipahami, sebab memungkinkan kita mempelajari sifat-sifat senyawa, dan cara-cara yang digunakan untuk membuat ikatan kimia.

Penyingkatan Konfigurasi Elektron dengan Konfigurasi Gas Mulia YouTube
Nah sekarang kita akan menggambarkan konfigurasi elektron memakai diagram orbital, teman. Sebenarnya gambarnya cukup mudah kok. Suatu subkulit punya sejumlah orbital. Orbital itu digambarkan sebagai persegi dan berisi garis setengah panah yang mewakili elektron. Subkulit s punya 1 orbital, p punya 3 orbital, d punya 5 orbital, dan f 14 orbital.

Kimia kelas 10 kestabilan konfigurasi elektron dengan notasi gas mulia YouTube
Konfigurasi Elektron Gas Mulia. Gas mulia adalah unsur-unsur yang memiliki kestabilan yang sangat tinggi dan dalam sistem periodik terdapat pada golongan VIIIA.. Berikut ini adalah konfigurasi elektron dari unsur gas mulia. 2 He = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6.
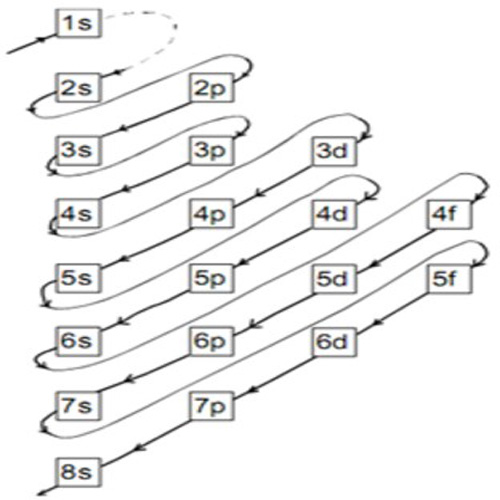
Pengertian Konfigurasi Elektron Rumus Kimia
Konfigurasi Elektron Gas Mulia. Gas mulia merupakan kelompok unsur yang sangat stabil (sulit bereaksi) karena konfigurasi elektron valensinya yang penuh (elektron valensi akan dibahas di pembahasan selanjutnya). Unsur-unsur yang termasuk gas mulia adalah helium (He), neon (Ne), argon (Ar), kripton (Kr), xenon (Xe), dan radon (Rn). Berikut.
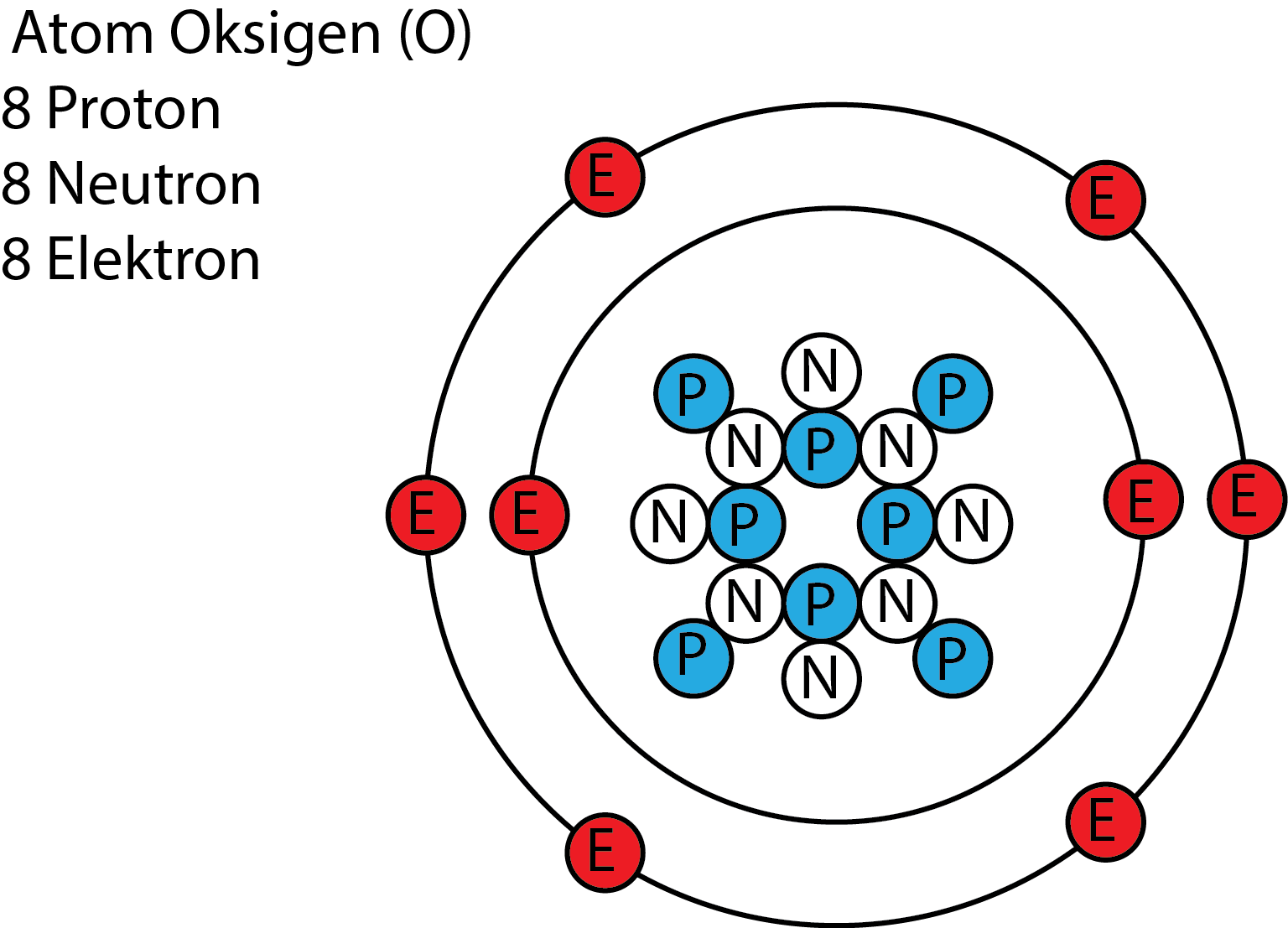
Bagaimana Konfigurasi Elektron Gas Mulia Dan Struktur
Sifat - Sifat Gas Mulia. Konfigurasi elektron untuk gas mulia berakhiran 2 dan 8 yang merupakan suatu bentuk konfigurasi elektron yang stabil. Ini yang menyebabkan golongan ini stabil (sukar bereaksi dengan unsur lain). Dari atas ke bawah potensial ionisasinya ialah makin kecil, reaktifitasnya makin besar, titik didih dan titik leleh makin besar.

GAS MULIA Pengertian, Sifat, Keberadaan, Cara Pembuatan dan Kegunaannya
Konfigurasi Elektron Gas Mulia. Gas mulia adalah gas golongan VIIIA yang cukup stabil, sehingga sulit untuk bereaksi dengan unsur lain. Golongan unsur gas mulia terdiri dari He (helium), Ne (neon), Ar (argon), Kr (kripton), Xe (xenon), dan Rn (radon). Adapun konfigurasi gas mulia tersebut adalah sebagai berikut. 2 He = 1s 2; 10 Ne = 1s 2 2s 2.

Aturan Konfigurasi Elektron Dan Diagram Orbital Superprof
Konfigurasi elektron gas mulia tergolong konfigurasi elektron penuh dan merupakan bentuk konfigurasi elektron yang paling stabil dengan elektron valensi berjumlah 8 (oktet) kecuali elektron valensi He yang berjumlah 2 (duplet). Konfigurasi elektron gas mulia secara lengkap tersedia dalam tabel berikut. Tabel Konfigurasi Elektron Gas Mulia Unsur Kulit n = 1 n = 2 n =
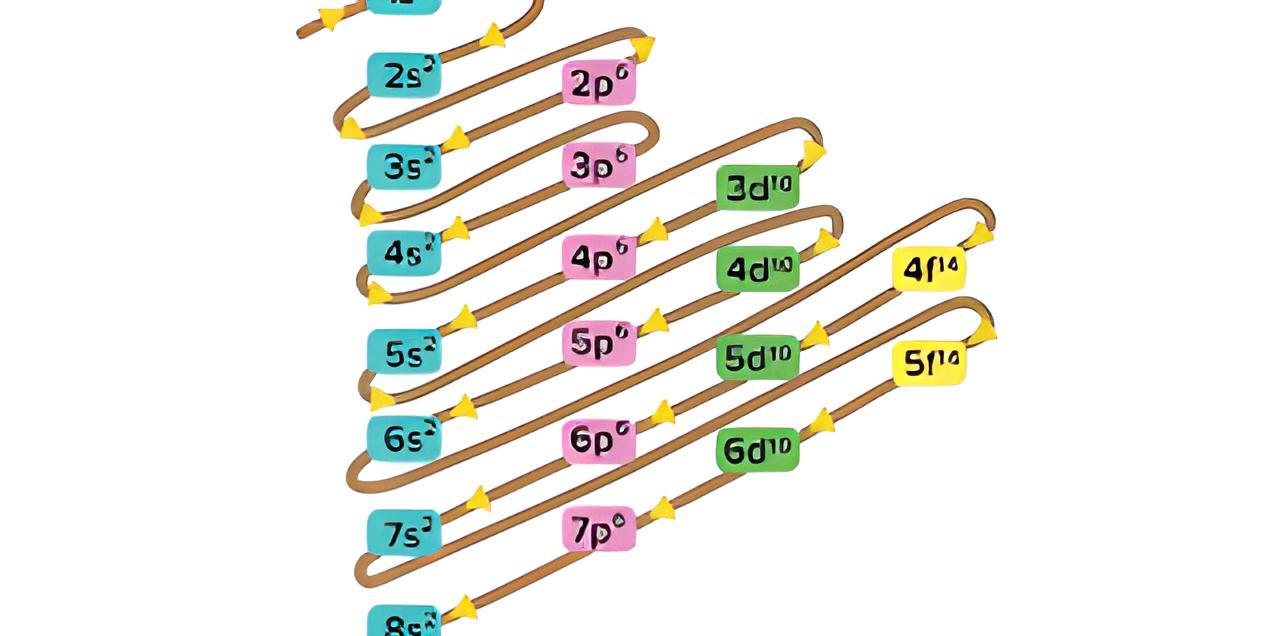
Aturan Konfigurasi Elektron Dan Diagram Orbital Superprof
Konfigurasi elektron yang pertama kali dipikirkan adalah berdasarkan pada model atom model Bohr.Adalah umum membicarakan kelopak maupun subkelopak walaupun sudah terdapat kemajuan dalam pemahaman sifat-sifat mekanika kuantum elektron. Berdasarkan asas larangan Pauli, sebuah orbital hanya dapat menampung maksimal dua elektron.Namun pada kasus-kasus tertentu, terdapat beberapa orbital yang.

Konfigurasi Elektron Untuk Ion Cu Konfigurasi Elektron
Karena gas mulia memiliki konfigurasi elektron yang stabil maka gas mulia juga biasa digunakan untuk menyingkat konfigurasi elektron unsur-unsur lain. Konfigurasi elektron menggunakan gas mulia ditunjukkan pada tabel konfigurasi elektron berikut ini. Tabel Konfigurasi Elektron Menggunakan Gas Mulia Unsur Nomor Atom Konfigurasi Elektron Litium (Li) 3 [He] 2s1 Berilium (Be) 4 [He] 2s2 Boron (B)

Konfigurasi Elektron
Gas mulia memiliki kestabilan yang sangat tingi akibat proses konfigruasi elektron yang terjadi di dalamnya. Berikut ini adalah konfigurasi elektron dari unsur gas mulia: 2He = 1s2. 10Ne = 1s2 2s2 2p6. 18Ar = 1s2 2s2 2p6 3s2 3p6.

Bagaimana Konfigurasi Elektron Gas Mulia Dan Struktur
Konfigurasi Elektron Gas Mulia. Gas mulia adalah unsur-unsur yang memiliki kestabilan yang sangat tinggi dan dalam sistem periodik terdapat pada golongan VIIIA. Yang terdiri dari He. Berikut ini adalah konfigurasi elektron dari unsur gas mulia. 2 He = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4f 14 5d 10 6p 6;
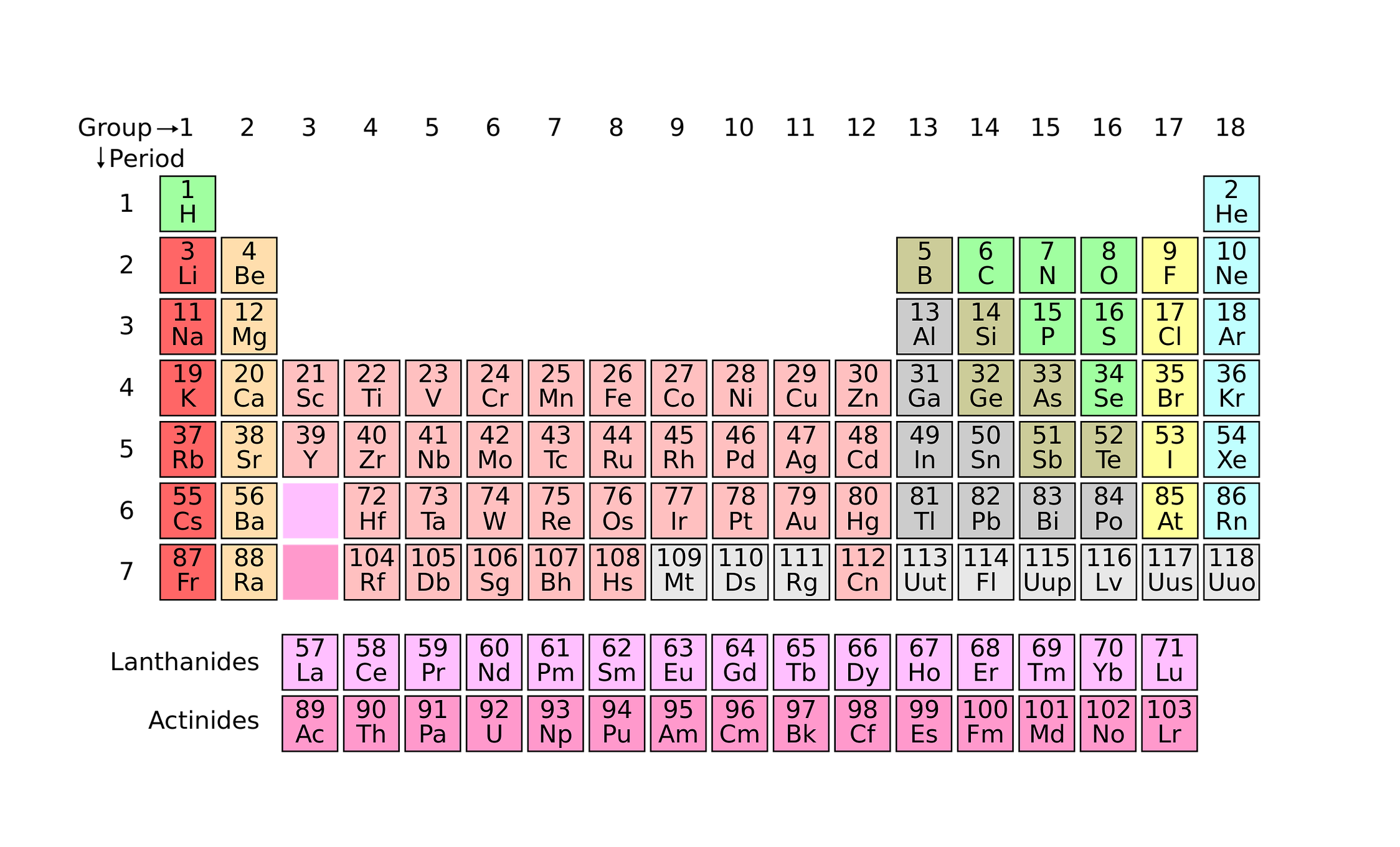
Kimia Mengenal Gas Mulia dan Sifatsifatnya Ngaji Galileo
Hal penting yang membuat golongan unsur yang termasuk ke dalam gas mulia ini mempunyai kestabilan yang tinggi yaitu karena konfigurasi dari elektron yang dimilikinya. Selain itu, konfigurasi dari gas mulia juga biasa digunakan untuk menyingkat konfigurasi unsur lainnya. Contohnya yaitu ketika akan menulis konfigurasi dari elektron unsur 21 Sc.